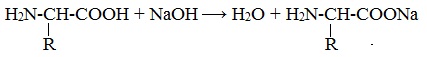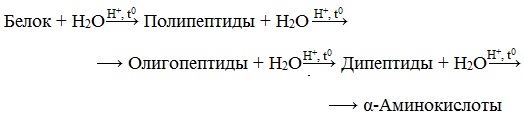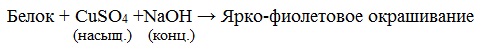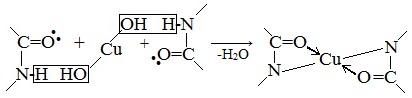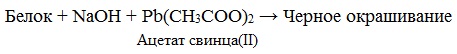СУББОТА, 28.05.22 г. 408,305,406
ГРУППА 408 ХИМИЯ 59,60
ТЕМА: Химические свойства карбоновых кислот
Карбоновые кислоты проявляют высокую реакционную способность. Они вступают в реакции с различными веществами и образуют разнообразные соединения, среди которых большое значение имеют функциональные производные, т.е. соединения, полученные в результате реакций по карбоксильной группе.
I. Общие с другими кислотами
1. Диссоциация:
R-COOH ↔ RCOO- + H+
-Сила кислот уменьшается в ряду:
H-COOH > CH3-COOH > CH3-CH2-COOH
ВИДЕО:
Растворимостьв воде различных карбоновых кислот
Карбоновыекислоты - слабые электролиты
2. Взаимодействие с активными металлами:
2R-COOH + 2Na → 2R-COONa + H2↑
ВИДЕО:
Взаимодействиеуксусной кислоты с металлами
3. Взаимодействие с основными оксидами и основаниями:
2R-COOH + CaO → (R-COO)2Ca + H2O
ВИДЕО:
Взаимодействиеуксусной кислоты с оксидом меди (II)
R-COOH + NaOH → R-COONa + H2O
ВИДЕО:
Взаимодействиеуксусной кислоты с раствором щелочи
4. Взаимодействие с солями слабых кислот:
R-COOH + NaHCO3 → R-COONa + H2O + CO2↑
ВИДЕО:
Взаимодействиеуксусной кислоты с карбонатом натрия
-Соли карбоновых кислот разлагаются сильными минеральными кислотами:
R-COONa + HСl → NaCl + R-COOH
-В водных растворах гидролизуются:
R-COONa + H2O ↔ R-COOH + NaOH
ВИДЕО:
5. Образование сложных эфиров со спиртами:
II. Специфические свойства
1. Образование функциональных производных R-CO-X
(свойства гидроксильной группы)
Получение хлорангидридов:
R-COOH + PCl5 → R-CO-Cl + POCl3 + HCl
2. Образование амидов
CH3COOH + NH3→CH3COONH4 t˚C→ CH3CONH2 + H2O
Вместо карбоновых кислот чаще используют их галогенангидриды:
Амиды образуются также при взаимодействии карбоновых кислот (их галогенангидридов или ангидридов) с органическими производными аммиака (аминами):
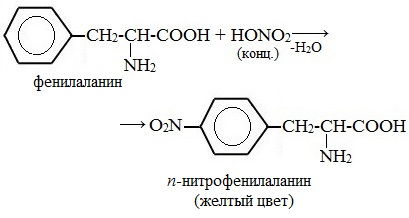
Амиды играют важную роль в природе. Молекулы природных пептидов и белков построены из a-аминокислот с участием амидных групп - пептидных связей
3. Реакции замещения с галогенами
(свойства углеводородного радикала, образуется а-хлорпроизводное карбоновой кислоты ):
4. Особенности муравьиной кислоты H-COOH:
· Даёт реакцию «Серебряного зеркала»:
H-COOH + 2[Ag(NH3)2]OH → 2Ag↓ + (NH4)2CO3 + 2NH3 + H2O
· Окисление хлором:
H-COOH + Cl2 → CO2 + 2HCl
· Вступает в реакцию с гидроксидом меди(II):
H-COOH + 2Cu(OH)2 t → Cu2O↓ + CO2↑ + 3H2O
· Разлагается при нагревании:
HCOOH t,H2SO4→ CO↑ + H2O
ВИДЕО:
5. Реакции декарбоксилирования солей карбоновых кислот
(получение алканов):
R-COONa + NaOH t → Na2CO3 + R-H (алкан)
6. Окисление в атмосфере кислорода:
R-COOH + O2 → CO2 + H2O
ВИДЕО:
ВИДЕО:
Взаимодействие бромной воды с олеиновой кислотой
Окислениемуравьиной кислоты раствором перманганата калия
Получение и применение карбоновых кислот
Получение карбоновых кислот I. В промышленности 1. Выделяют из природных продуктов (жиров, восков, эфирных и растительных масел) 2. Окисление алканов: 2CH4 + + 3O2 t,kat → 2HCOOH + 2H2O метан муравьиная кислота 2CH3-CH2-CH2-CH3 + 5O2 t,kat,p → 4CH3COOH + 2H2O н-бутан уксусная кислота 3. Окисление алкенов: CH2=CH2 + O2 t,kat → CH3COOH этилен СH3-CH=CH2 + 4[O] t,kat → CH3COOH + HCOOH (уксусная кислота+муравьиная кислота) 4. Окисление гомологов бензола (получение бензойной кислоты): C6H5-CnH2n+1 + 3n[O] KMnO4,H+→ C6H5-COOH + (n-1)CO2 + nH2O 5C6H5-CH3 + 6KMnO4 + 9H2SO4 → 5C6H5-COOH + 3K2SO4 + 6MnSO4 + 14H2O толуол бензойная кислота 5. Получение муравьиной кислоты: 1 стадия: CO + NaOH t,p → HCOONa (формиат натрия – соль) 2 стадия: HCOONa + H2SO4 → HCOOH + NaHSO4 6. Получение уксусной кислоты: CH3OH + CO t,p → CH3COOH Метанол II. В лаборатории 1. Гидролиз сложных эфиров: 2. Из солей карбоновых кислот: R-COONa + HCl → R-COOH + NaCl 3. Растворением ангидридов карбоновых кислот в воде: (R-CO)2O + H2O → 2 R-COOH 4. Щелочной гидролиз галоген производных карбоновых кислот: III. Общие способы получения карбоновых кислот 1. Окисление альдегидов: R-COH + [O] → R-COOH Например, реакция «Серебряного зеркала» или окисление гидроксидом меди (II) – качественные реакции альдегидов 2. Окисление спиртов: R-CH2-OH + 2[O] t,kat → R-COOH + H2O 3. Гидролиз галогензамещённых углеводородов, содержащих три атома галогена у одного атома углерода. 4. Из цианидов (нитрилов) – способ позволяет наращивать углеродную цепь: СH3-Br + Na-C≡N → CH3-CN + NaBr CH3-CN - метилцианид ( нитрил уксусной кислоты) СH3-CN + 2H2O t → CH3COONH4 ацетат аммония CH3COONH4 + HCl → CH3COOH + NH4Cl 5. Использование реактива Гриньяра R-MgBr + CO2 → R-COO-MgBr H2O → R-COOH + Mg(OH)Br ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ Муравьиная кислота – в медицине - муравьиный спирт (1,25% спиртовой раствор муравьиной кислоты), в пчеловодстве, в органическом синтезе, при получении растворителей и консервантов; в качестве сильного восстановителя. Уксусная кислота – в пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров). В домашнем хозяйстве как вкусовое и консервирующее вещество. Масляная кислота – для получения ароматизирующих добавок, пластификаторов и флотореагентов. Щавелевая кислота – в металлургической промышленности (удаление окалины). Стеариновая C17H35COOH и пальмитиновая кислота C15H31COOH – в качестве поверхностно-активных веществ, смазочных материалов в металлообработке. Олеиновая кислота C17H33COOH – флотореагент и собиратель при обогащении руд цветных металлов. ВИДЕО: Взаимодействие бромной воды с олеиновой кислотой СН2=СН-СООН + HCl → СН2Сl-СН2-СООН СН2=СН-СООН + Н2O → НО-СН2-СН2-СООН Две последние реакции протекают против правила Марковникова. Непредельные карбоновые кислоты и их производные способны к реакциям полимеризации. |
ГРУППА 408 БИОЛОГИЯ 46
ТЕМА: Чарльз Дарвин и его теория происхождения видов.
Тема: Чарльз Дарвин и его теория происхождения видов.
История развития и происхождения человеческого вида на протяжении столетий волнует учёных и множество обычных людей. Во все времена на этот счёт выдвигались всевозможные теории.
РОДИВШИЙСЯ В СЕМЬЕ ВРАЧА, ЧАРЛЬЗ ДАРВИН, ОБУЧАЯСЬ В КЕМБРИДЖЕ И ЭДИНБУРГЕ, СТАЛ ОБЛАДАТЬ ГЛУБОКИМИ ПОЗНАНИЯМИ В ОБЛАСТИ ГЕОЛОГИИ, БОТАНИКИ И ЗООЛОГИИ, А ТАКЖЕ ОВЛАДЕЛ НАВЫКАМИ ПОЛЕВЫХ ИССЛЕДОВАНИЙ, К КОТОРЫМ ИСПЫТЫВАЛ ТЯГУ.
Огромное влияние на формирование мировоззрения Дарвина, как учёного, оказал труд «Принципы геологии» Чарльза Лайеля – английского геолога. Согласно его мнению, современный вид нашей планеты постепенно формировался под воздействием тех же естественных сил, которые продолжают воздействовать и в наши дни. Чарльз Дарвин, естественно, был знаком с идеями Жана Батиста Ламарка, Эразма Дарвина и некоторых других эволюционистов раннего периода, но ни одна из них не подействовала на него, как теория Лайлея.
Однако поистине судьбоносную роль в судьбе Дарвина сыграло его странствие на судне «Бигль», проходившее с 1832 по 1837 годы. Сам Дарвин говорил, что самое больше впечатление на него произвели следующие открытия:
- Открытие ископаемых животных гигантских размеров и покрытых панцирем, который был похож на панцирь знакомых всем нам броненосцев;
- Очевидность того, что виды животных, близких по роду, замещают друг друга по мере продвижения по южноамериканскому материку;
- Очевидность того, что виды животных на различных островах Галапагосского архипелага лишь немногими отличаются друг от друга.
Впоследствии учёный заключил, что вышеназванные факты, как и множество других, могут быть объяснены лишь если предположить, что каждый из видов претерпевал постоянные изменения.
После того как Дарвин вернулся из путешествия, он занялся обдумыванием проблемы происхождения видов. Идей рассматривалось множество, в том числе, и идея Ламарка, но все они были отброшены за отсутствием объяснений поразительной способности растений и животных приспосабливаться к условиям среды обитания. Этот факт, который ранние эволюционисты считали не требующим обоснований, стал для Дарвина наиболее важным вопросом. Так он начал собирать информацию на тему изменчивости растений и животных в природных и домашних условиях.
Много лет спустя, вспоминая о возникновении своей теории, Дарвин писал, что совсем скоро он осознал, что главное значение в успешном создании человеком полезных видов растений и животных имел именно отбор. Хотя, на протяжении определённого времени учёный всё ещё не мог понять, как отбор может быть применимым к тем организмам, которые живут в естественной среде.
Именно в этот период в научных кругах Англии активно обсуждались идеи Томаса Мальтуса – английского учёного и демографа, который говорил о том, что популяция населения растёт в геометрической прогрессии. После прочтения его работы «О народонаселении» Дарвин продолжил свою предыдущую мысль, сказав, что продолжительные наблюдения за образом жизни растений и животных подготовили его к оценке значения вездесущей борьбы за существование. Но он был поражён мыслью, что благоприятные изменения в таких условиях должны оставаться и сохраняться, а неблагоприятные должны быть подвергнуты уничтожению. Итогом всего этого процесса и должно быть появление новых видов.
В результате, в 1838 году у Дарвина появилась теория происхождения видов посредством естественного отбора. Однако публикация этой теории состоялась лишь в 1859 году. А поводом для публикации послужили довольно-таки драматические обстоятельства.
В 1858 году человек по имени Альфред Уоллес – молодой британский биолог, натуралист и путешественник прислал Дарвину рукопись своей статьи «О тенденции разновидностей к неограниченному отклонению от первоначального типа». В данной статье было представлено изложение теории происхождения видов через естественный отбор. Дарвин решил не публиковать свой труд, но его соратники Чарльз Лайель и Джозеф Долтон Гукер, уже давно знавшие об идеях своего товарища и знакомые с набросками его работы, смогли убедить Дарвина, что публикация работы должна состояться одновременно с публикацией работы Уоллеса.
Так, в 1959 году вышла в свет работа Чарльза Дарвина «Происхождение видов путём естественного отбора, или Сохранение благоприятных рас в борьбе за жизнь», и её успех был просто ошеломительным. Теория Дарвина была прекрасно принята и поддержана одними учёными и жёстко раскритикована другими. Но все последующие труды Дарвина, как и этот, после публикации мгновенно приобретали статус бестселлеров и издавались на многих языках. Сам же учёный в мгновение ока приобрёл мировую известность.
И одной из причин популярности теории Дарвина явились её базовые принципы.
ГЛАВНЫЕ ПРИНЦИПЫ ТЕОРИИ ПРОИСХОЖДЕНИЯ ВИДОВ ЧАРЛЬЗА ДАРВИНА
Вся суть теории происхождения видов Дарвина заключается в комплексе положений, являющихся логичными, способных быть проверенными экспериментально и подтверждённых фактами. Этими положениями являются следующие:
- Любой вид живых организмов включает в себя огромнейший спектр индивидуальной генетической изменчивости, которая может различаться морфологическими, физиологическими, поведенческими и любыми другими признаками. Эта изменчивость может быть непрерывного количественного или прерывистого качественного характера, однако существует в любой момент времени. Найти двух особей, которые были бы абсолютно идентичны по совокупности признаков, невозможно.
- У любого живого организма есть способность быстро увеличивать популяцию. Не может быть никакого исключения из правила, говорящего о том, что органические существа размножаются в такой прогрессии, что если бы они не истреблялись, то одна пара могла бы покрыть потомством всю планету.
- Для любого вида животных имеются только ограниченные ресурсы для жизни. По этой причине большое производство особей должно служить катализатором борьбы за существование либо между представителями одного вида, либо между представителями различных видов, либо с условиями существования. Борьба за существование, согласно теории Дарвина, включает в себя как борьбу представителя какого-либо вида за жизнь, так и его борьбу за успешное обеспечение себя потомством.
- В борьбе за существование способны выжить и успешно производить потомство только самые приспособленные особи, которые имеют особые отклонения, оказавшиеся адаптивными к конкретным условиям среды обитания. Причём, такие отклонения возникают именно случайно, а не реагируя на воздействие среды. И полезность этих отклонений также случайна. Отклонение передаётся потомкам особи, которая выжила, на генетическом уровне, по причине чего они становятся более адаптированными к имеющейся среде обитания, нежели другие особи того же вида.
- Естественный отбор представляет собой процесс выживания и преимущественного размножения приспособленных представителей популяции. Естественный отбор, по словам Дарвина, точно так же постоянно фиксирует любые изменения, сохраняет хорошие и отбрасывает плохие, как это делает селекционер, изучающий множество особей и отбирающий и размножающий лучше из них.
- Применительно к отдельным изолированным разновидностям в различных условиях жизни, естественный отбор приводит к расхождению их признаков и, в итоге, к образованию нового вида.
Данные положения, являющиеся практически безупречными с точки зрения логики, и подкреплённые большим количеством фактического материала, являются основой теории эволюции, которую мы можем видеть сегодня.
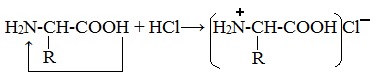
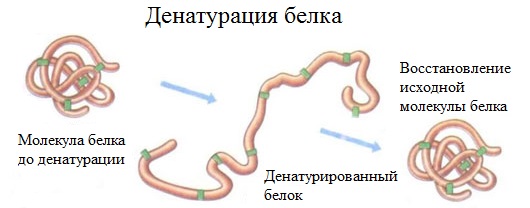
ГРУППА 305 ХИМИЯ 46,47 ТЕМА: Растворение белков в воде. Обнаружение белков в молоке и в мясном бульоне. Химические свойства глюкозы, сахарозы, крахмала. Изучение свойств белков. ТЕМА: Биологические функции белков. Химические свойства белков: горение, денатурация, гидролиз, цветные реакции. Растворение белков в воде. Обнаружение белков в молоке и в мясном бульоне. Изучение свойств белков. ТЕМА: Растворение белков в воде. Обнаружение белков в молоке и в мясном бульоне. Химические свойства глюкозы, сахарозы, крахмала. Изучение свойств белков. По химическому составу белки делятся на две группы: а) простые белки – протеины, которые при гидролизе распадаются только на аминокислоты; б) сложные белки или протеиды, образующие при гидролизе аминокислоты и вещества небелковой природы (углеводы, нуклеиновые кислоты и др.) — соединения белковых веществ с небелковыми. 1. Амфотерные свойства белковКак и аминокислоты, белки являются амфотерными соединениями, так как молекула любого белка содержит на одном конце группу -NH2, а на другом конце – группу -СООН. Так, при действии щелочей белок реагирует в форме аниона – соединяется с катионом щелочи: При действии же кислот он выступает в форме катиона: Если в молекуле белка преобладают карбоксильные группы, то он проявляет свойства кислот, если же преобладают аминогруппы, — свойства оснований. Очень важным для жизнедеятельности живых организмов является буферное свойство белков, т.е. способность связывать как кислоты, так и основания, и поддерживать постоянное значение рН различных систем живого организма. Белки обладают и специфическими физико-химическими свойствами. 2. Денатурация белка (необратимое осаждение, свертывание)Денатурация – это разрушение вторичной и третичной структуры белка (полное или частичное) и изменение его природных свойств с сохранением первичной структуры белка. Сущность денатурации белка сводится к разрушению связей, обусловливающих вторичную и третичную структуры молекулы (водородных, солевых и других мостиков). А это приводит к дезориентации конфигурации белковой молекулы. Денатурация бывает обратимой и необратимой. Обратимая денатурация белка происходит при употреблении алкоголя, солёной пищи. Необратимая денатурация может быть вызвана при действии таких реагентов, как концентрированные кислоты и щелочи, спирты, в результате воздействия высокой температуры, радиации, при отравлении организма солями тяжелых металлов (Hg2+, Pb2+, Си2+). Например, яичный белок альбумин осаждается из раствора (свертывается) при варке яиц (при температуре 60-700С), теряя способность растворяться в воде. Видеоопыт «Свертывание белков при нагревании» Видеоопыт «Осаждение белков солями тяжелых металлов» Видеоопыт «Осаждение белков спиртом» 3. Гидролиз белковГидролиз белков – это необратимое разрушение первичной структуры в кислом или щелочном растворе с образованием аминокислот. Анализируя продукты гидролиза, можно установить количественный состав белков. Переваривание белков в организме по своей сути представляет ферментативный гидролиз белковых молекул. В лабораторных условиях и в промышленности проводится кислотный гидролиз. В ходе гидролиза белков происходит разрушение пептидных связей. Гидролиз белка имеет ступенчатый характер: |