13.10.22 г. ЧЕТВЕРГ. 508, 405,303
Здравствуйте, уважаемые студенты, записывайте дату, тему и выполняйте необходимые записи (ВСЁ подряд не пишите, читайте, выбирайте, можно составить план, ЕСЛИ ЕСТЬ ВИДЕО, НАДО ПОСМОТРЕТЬ ,ВЫПОЛНИТЬ ПО НЕМУ ЗАПИСИ, МНОГО НЕ НУЖНО ПИСАТЬ. Материала может быть выложено много, но это не значит, что всё надо записывать! После этого, сфотографируйте и отошлите мне на почту rimma.lu@gmail.com . Тетрадь привезете, когда перейдем на очную форму обучения.)
Справа находится АХИВ БЛОГА , смотрите дату и номер своей группы
моя почта : rimma.lu@gmail.com Жду ваши фотоотчеты!
ГРУППА 508 БИОЛОГИЯ 6,7
ТЕМА 6,7: Нуклеиновые кислоты.
СНАЧАЛА ВНИМАТЕЛЬНО ПОСМОТРИТЕ ВИДЕО. ЗАТЕМ ПРОЧИТАЙТЕ НИЖЕ ТЕКСТ, ЗАПИШИТЕ ГЛАВНОЕ.
Строение нуклеиновых кислот
В отличие от белков, углеводов и липидов, нуклеиновые кислоты никогда не накапливаются в клетке в больших количествах, и обнаружить их можно только с помощью специальных химических методов. Поэтому они были открыты только во второй половине XIX в., а по-настоящему изучить их роль в процессах жизнедеятельности удалось лишь во второй половине XX в. Так как первоначально они были обнаружены только в ядрах, им дали название нуклеиновые (от лат. nucleus — ядро).
Нуклеиновые кислоты — биологические полимеры, мономерами которым служат нуклеотиды. Связи между нуклеотидами легко подвергаются гидролизу (распаду при реакции с водой). Каждый нуклеотид состоит из остатков углевода, фосфорной кислоты и азотистого основания (рис. 1).

Рис. 1. Строение нуклеотида
Углеводный компонент представлен пентозами — рибозой (в РНК) или дезоксирибозой (в ДНК), у которой отсутствует кислород при втором атоме углерода (рис. 2).

Рис. 2. Пентозы
Остаток фосфорной кислоты образует сложноэфирную связь с гидроксилом при 5-м атоме углерода в сахаре. Соединение нуклеотидов в полимер происходит путем образования фосфатом одного нуклеотида второй эфирной связи с гидроксилом при 3-м углероде соседнего нуклеотида. Такая связь получила название фосфодиэфирной.
Таким образом, нуклеиновые кислоты представляют собой цепь из чередующихся остатков пентозы и фосфорной кислоты (рис. 3).
Кроме того, от первого атома углерода каждой пентозы отходит в бок азотистое основание. В этом нуклеиновые кислоты сходны с белками, в которых полимерная цепь образована пептидными группировками с отходящими от них боковыми радикалами аминокислот. Так же, как и у белков, в нуклеиновых кислотах два конца цепи неодинаковы. С одной стороны имеется не занятое связью пятое положение рибозы, этот конец называют 5’-концом. С противоположной стороны не занят связью третий гидроксил сахара, этот конец обозначают как 3’-конец. 5’-конец считается началом цепи, а 3’-конец — ее окончанием.

Рис. 3. Нуклеиновые кислоты
В одной молекуле нуклеиновой кислоты присутствует только один вид пентозы. Те молекулы, которые содержат рибозу, называют рибонуклеиновой кислотой, или сокращенно РНК. Нуклеиновую кислоту, содержащие дезоксирибозу, называют дезоксирибонуклеиновой кислотой, или ДНК.
Помимо пентозы, нуклеиновые кислоты отличаются азотистыми основаниями. Они представляют собой ароматические циклы, содержащие несколько атомов азота и заместители при определенных атомах углерода.
По структуре гетероциклов азотистые основания делятся на две группы.
Пиримидиновые азотистые основания: урацил, тимин и цитозин. Тимин отличается от урацила только наличием метильной группы, что незначительно меняет его свойства. В РНК встречаются урацил и цитозин, а в ДНК — тимин и цитозин.
Пуриновые основания: аденин и гуанин. Во всех нуклеиновых кислотах присутствуют оба пурина.

Рис. 4. Азотистые основания
За счет чередования различных нуклеотидов в цепи нуклеиновые кислоты могут достигать огромного многообразия (количество видов полимеров равно числу видов мономеров в степени, равной числу мономеров в цепи). И хотя число мономеров в нуклеиновых кислотах меньше, чем в белках, степень полимерности, особенно у ДНК, намного выше. Длина цепей ДНК, входящих в хромосомы разных организмов, составляет от миллионов до сотен миллионов нуклеотидов.
Молекулы РНК обычно короче, их длина — от нескольких десятков до нескольких десятков тысяч нуклеотидов. А при длине цепи 500 нуклеотидов количество возможных комбинаций составляет более 10 300.
принцип комплЕментарности
При анализе содержания азотистых оснований в ДНК из различных организмов Эрвин Чаргафф обнаружил определенные закономерности, позднее названные правилами Чаргаффа.
Молярное содержание аденина всегда равно молярному содержанию тимина, а молярное содержание гуанина — молярному содержанию цитозина.
Количество пуринов равнялось количеству пиримидинов, а отношение А+Т/Г+Ц было различным у разных видов живых организмов.
Это указывало на возможные взаимодействия оснований в ДНК между собой.
На основании правил Чаргаффа и предварительных результатов рентгеноструктурного анализа Джеймс Уотсон и Френсис Крик в 1953 г. предложили двуспиральную модель структуры ДНК.
Согласно этой модели молекула ДНК состоит из двух полинуклеотидных цепей, соединенных между собой азотистыми основаниями. При этом аденин одной цепи всегда взаимодействует с тимином в другой, и наоборот. Точно так же гуанин одной цепи всегда связан с цитозином в другой (рис. 6).

Рис. 5. Образование водородных связей между азотистыми основаниями
Такие пары оснований удерживаются за счет образования между основаниями водородных связей:
- пара А–Т образует 2 водородные связи;
- пара Г–Ц образует 3 водородные связи.
Главной особенностью пар А–Т и Г–Ц является их одинаковая геометрия. Это позволяет построить двуспиральную молекулу с постоянным расстоянием между цепями, построенными остатками сахара и фосфорной кислоты. Образование любых других пар приводит к нарушению правильной структуры.
Такое взаимодействие оснований, при котором они дополняют друг друга до определенной структуры, одинаковой для всех пар, получило название принципа комплементарности.
Пары аденин и тимин, гуанин и цитозин называются комплементарными парами, а две цепочки нуклеиновых кислот, в которых все основания образуют комплементарные пары — комплементарными цепочками. Таким образом, каждая молекула ДНК состоит из двух комплементарных цепочек полинуклеотидов (рис. 6).

Рис. 6. Принцип комплиментарности
Важной особенностью структуры двойной спирали ДНК является то, что комплементарные цепи направлены в противоположные стороны, т. е. 5’-конец одной цепи связан комплементарными основаниями с 3’-концом другой цепи, и наоборот. Основания плотно слипаются своими плоскостями, что делает связь между цепочками еще более прочной. Такое слипание получило название стэкинг-взаимодействия. В результате в центре молекулы ДНК находится как бы стержень, построенный из азотистых оснований, а по краям он обвит двумя нитями, состоящими из чередующихся остатков дезоксирибозы и фосфорной кислоты.
сравнение ДНК и РНК
| Нуклеиновая кислота | Строение | Функции | Особенности |
| ДНК | азотистое основание: аденин (А) тимин (Т) гуанин (Г) цитозин (Ц) углевод: дезоксирибоза остаток фосфорной кислоты | хранение и передача наследственной информации | двойная спираль (по принципу комплементарности); способность к репликации (самоудвоению) |
| РНК | азотистое основание: аденин (А) урацил (У) гуанин (Г) цитозин (Ц) углевод: рибоза остаток фосфорной кислоты | биосинтез белка | одинарная цепочка нуклеотидов |
ГРУППА 405 ХИМИЯ 19,20
ТЕМА 19,20:Химические свойства алканов (метана, этана): горение, замещение, разложение, дегидрирование.Применение алканов на основе свойств. Ознакомление с коллекцией образцов нефти и продуктов ее переработки.
Физические и химические свойства алканов
Метан и его газообразные гомологи (до бутана включительно) содержатся в природном и попутном нефтяном газах. Жидкие алканы — основная часть нефти. Твёрдые предельные углеводороды (парафин) растворены в нефти, которая и служит источником их получения.
При обычных условиях алканы не реагируют с концентрированными кислотами и щелочами, не окисляются сильными окислителями, такими как перманганат калия.
Однако при нагревании химическое поведение алканов резко меняется. Все алканы горят бледно-голубым пламенем с образованием углекислого газа и воды:
Горение алканов сопровождается выделением большого количества теплоты, что определяет их использование в качестве топлива.
Следует помнить, что углеводороды относятся к пожаро- и взрывоопасным веществам. Утечка бытового газа грозит страшными последствиями. Для того чтобы вовремя обнаружить наличие в воздухе бытового газа, к нему добавляют вещества с резким неприятным запахом — одоранты. Если вы почувствовали на кухне, в подъезде или на улице запах газа, следует немедленно обратиться в экстренную службу по телефону 104, проветрить помещение и ни в коем случае не пользоваться открытым огнём или электроприборами. В случае пожара службу спасения вызывают по телефону 101 или 112 (с сотового телефона бесплатно).
Предельные углеводороды используют не только как топливо, но и в качестве сырья для химической промышленности, поскольку их свойства отнюдь не ограничиваются реакцией горения.
В предельных углеводородах атомы водорода могут замещаться другими атомами или группами, в частности атомами галогенов (хлора и брома). Эти реакции замещения протекают ступенчато при освещении смеси газов: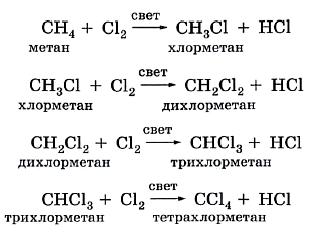
Галогенпроизводные алканов — прекрасные растворители, хладагенты (рабочие жидкости, которыми заправляют бытовые холодильники и промышленные холодильные установки), реагенты для органического синтеза.
Если предельные углеводороды нагревать без доступа воздуха при более высокой температуре, то они не выдерживают такого воздействия и разлагаются. Например, из метана при нагревании свыше 1000 °С образуется два ценных продукта — сажа (углерод) и водород:![]()
Сажу, полученную таким образом, используют для изготовления автомобильных шин и резины, она входит в состав красок и туши.
Алканы с неразветвлённой цепью углеродных атомов при нагревании превращаются в более устойчивые соединения с разветвлённой цепью. Например, из н-бутана можно получить изобутан:
Поскольку состав исходного вещества и продукта реакции одинаков, эти соединения являются изомерами. Именно поэтому такой процесс получил название реакция изомеризации.
При нагревании в присутствии катализатора алканы способны вступать в реакцию отщепления. Что же могут отщеплять молекулы предельных углеводородов? Если предположить, что углеродная цепь остаётся без изменения, то отщепляться могут только молекулы водорода.
| Реакцию, при которой от молекулы органического вещества отщепляется молекула водорода, называют реакцией дегидрирования. |
При дегидрировании этана образуются два продукта — этилен и водород:
Этилен С2Н4 — представитель непредельных углеводородов, о которых пойдёт речьПОЗЖЕ .
Тема: Применение алканов на основе свойств.
Области применения алканов связаны с их физико-химическими свойствами:
Таблица «Предельные углеводороды
(алканы, парафины)»

ГРУППА 405 экология 9
ТЕМА 9: ЧЕЛОВЕК КАК БИОСОЦИАЛЬНЫЙ ВИД.
ОТКРОЙТЕ УЧЕБНИК ЭКОЛОГИИ (это ссылка на электронный учебник.) СТР. 162-165 ПАРАГРАФ 23. ПРОЧИТАЙТЕ, СОСТАВЬТЕ ПЛАН ОТВЕТА.РАССМОТРИТЕ РИСУНКИ.
ГРУППА 303 ЭКОЛОГИЯ 1,2
Тема:1,2 Социально- экологические особенности демографии человека.
ОТКРОЙТЕ УЧЕБНИК ЭКОЛОГИИ (это ссылка на электронный учебник.) СТР. 195-201 ПАРАГРАФ 30. ПРОЧИТАЙТЕ, СОСТАВЬТЕ ПЛАН ОТВЕТА.РАССМОТРИТЕ РИСУНКИ, ОТВЕТЬТЕ письменно НА ВОПРОС 1 стр.201 .