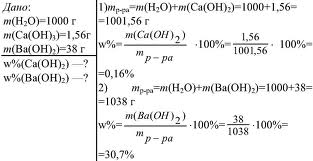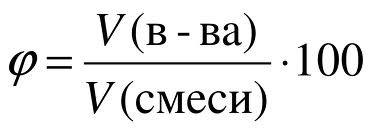20.02.21 г. 108, 305, 306 учимся за понедельник.
ГРУППА 108
ТЕМА: Химия и пища. Маркировки упаковок пищевых и гигиенических продуктов и умение их читать.
ОЗНАКОМИТЬСЯ И СОСТАВИТЬ КОНСПЕКТ ПО ПРЕЗЕНТАЦИИ
ГРУППА 305 ХИМИЯ
ТЕМА:
основные свойства кислот в свете теории электролитической диссоциации ( ТЭД)
Рассмотрим в свете ТЭД свойства веществ, растворы которых обладают электропроводностью
- одноосновные
- двухосновные
- многоосновные
ЗАДАНИЕ: прочитать текст, сделать записи , просмотреть видео, выполнить тесты.
Основные термины:
Массовая доля – отношение массы растворенного вещества к общей массе раствора.
Объемная доля – отношение объема данного вещества к общему объему смеси.
Ход урока:
1. Проверка изученного.
1. Среди приведенных объектов выберите самый маленький по размеру:
а) бактерия;
б) молекула;
в) маковое зернышко;
г) песчинка.
2. В каком ряду все перечисленные вещества относятся к простым?
а) мел, углерод, озон;
б) алмаз, кислород, гранит;
в) сера, фосфор, озон;
г) крахмал, водород, железо.
3. Очень важной для живой природы особенностью физических свойств воды является то, что:
а) температура кипения воды равна 100º С;
б) плотность жидкой воды выше плотности льда;
в) температура замерзания воды равна 0º С;
г) вода обладает очень низкой электропроводностью.
4. Соединений, содержащих только атомы водорода и кислорода:
а) не известно ни одного;
б) известно только одно;
в) известно несколько;
г) известно огромное количество.
5. При взаимодействии кислорода с металлами:
а) образуются соли;
б) выделяется озон;
в) образующиеся соединения всегда являются оксидами;
г) образующиеся соединения не всегда являются оксидами.
Растворы в природе.
Самые простые растворы состоят из двух компонентов. Один из компонентов раствора – растворитель. Для нас более привычны жидкие растворы, значит, растворитель в них – жидкое вещество. Чаще всего – вода.
Вы уже знаете, что природная вода никогда не бывает совершенно чистой. Так, существует вода, которая содержит значительное количество солей кальция и магния и называется жесткой (есть также мягкая вода, например дождевая). Жесткая вода дает мало пены с мылом, а на стенках котлов и чайников при ее кипячении образуется накипь. На рисунке 1 вы можете посмотреть, как жесткая вода образует накипь. Жесткость воды зависит от количества растворенных в ней солей. Содержание растворенного вещества в растворе выражают с помощью ее массовой доли.
Рис.1. Влияние жесткой воды
Другой компонент раствора – растворенное вещество. Им может быть и газ, и жидкое, и твердое вещество.
В ювелирных и технических изделиях применяют не чистое золото, а его сплавы, чаще всего с медью и серебром. Чистое золото — металл слишком мягкий, ноготь оставляет на нем след. износостойкость его невелика. Проба, стоящая на золотых изделиях, изготовленных в нашей стране, означает массовую долю золота в сплаве, точнее, содержание его из расчета на тысячу массовых частей сплава. Проба 583°, например, означает, что в сплаве массовая доля золота составляет 0,583 или 58,3%.
Массовая доля.
Один из самых распространенных способов выражения концентрации раствора – через массовую долю растворенного вещества.
Отношение массы растворенного вещества к общей массе раствора называют массовой долей растворенного вещества.
Массовую долю обозначают греческой буквой «омега» и выражают в долях единицы или процентах (рисунок 2).
Рис.2. Массовая доля компонентов смеси.
Посмотрев видео
вы вникнете в понятие массовой доли и научитесь ее вычислять.
Если в 100 г раствора содержится 30 г хлорида натрия, это означает, что ω(NaCl) = 0,3 или ω(NaCl) = 30 %. Можно также сказать: «имеется тридцатипроцентный раствор хлорида натрия».
Массовая доля — самая распространенная в быту и большинстве отраслей промышленности концентрация. Именно массовая доля жира, например, указана на пакетах с молоком (посмотрите на рисунок 3).
Рис.3. Массовая доля жира в молоке.
Масса раствора складывается из массы растворителя и массы растворенного вещества, т. е.:
m(раствора) = m(растворителя) + m(растворенного вещества).
Предположим, массовая доля растворенного вещества равна 0,1, или 10%. Следовательно, оставшиеся 0,9, или 90%, – это массовая доля растворителя.
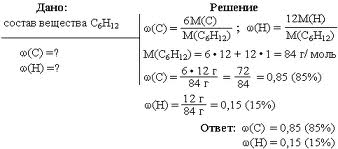
Массовая доля растворенного вещества широко используется не только в химии, но и в медицине, биологии, физике, да и в повседневной жизни. Рассмотрим решение некоторых задач, представленных на рисунке 4 и 5.
Рис.4. Задача на нахождение массовой доли.
Рис.5. Задача на нахождение массовой доли (в процентах).
Объемная доля.
В состав воздуха входит несколько различных газов: кислород, азот, углекислый газ, благородные газы, водяные пары и некоторые другие вещества. Содержание каждого из этих газов в чистом воздухе строго определенно.
Для того чтобы выразить состав смеси газов в цифрах, т.е. количественно, используют особую величину, которую называют объемной долей газов в смеси.
Аналогично массовой доле определяется и объемная доля газообразного вещества в газовой смеси, обозначаемая греческой буквой фи (рисунок 6):
Рис. 6. Объемная доля.
Объемная доля газа показывает, какую часть общего объема смеси занимает данный газ.
Если бы нам удалось разделить 100 л воздуха на отдельные газообразные компоненты, мы получили бы около 78 л азота, 21 л кислорода, 30 мл углекислого газа, в оставшемся объеме содержались бы так называемые благородные газы (главным образом аргон) и некоторые другие (рисунок 7).
Рис.7. Объемная доля благородных газов в воздухе.
Тот воздух, который мы выдыхаем, гораздо беднее кислородом (его объемная доля снижается до 16%), зато содержание углекислого газа возрастает до 4%. Такой воздух для дыхания уже непригоден. Вот почему помещение, в котором находится много людей, надо регулярно проветривать.
В химии на производстве чаще приходится сталкиваться с обратной задачей: определять объем газа в смеси по известной объемной доле.
Давайте посмотрим, как решать задачи на нахождение объемной доли (рисунок 8).
Рис.8. Задача на нахождение объемной доли.
Выводы.
1. Самые простые растворы состоят из двух компонентов. Один из компонентов раствора – растворитель. Для нас более привычны жидкие растворы, значит, растворитель в них – жидкое вещество. Другой компонент раствора – растворенное вещество. Им может быть и газ, и жидкое, и твердое вещество.
2. Один из самых распространенных способов выражения концентрации раствора – через массовую долю растворенного вещества. Отношение массы растворенного вещества к общей массе раствора называют массовой долей растворенного вещества. Массовую долю обозначают греческой буквой «омега» и выражают в долях единицы или процентах.
3. Объемная доля газа показывает, какую часть общего объема смеси занимает данный газ. Объемная доля газообразного вещества в газовой смеси обозначается греческой буквой фи.
Контролирующий блок.
1. Что такое массовая доля растворенного вещества?
2. Что такое объемная доля компонента в газовой смеси?
3. Сравните понятия «объемная доля» и «массовая доля» компонентов смеси.