10.10.22г. ПОНЕДЕЛЬНИК 501,408,406,405
Здравствуйте, уважаемые студенты, записывайте дату, тему и выполняйте необходимые записи(ВСЁ подряд не пишите, читайте, выбирайте, можно составить план, ЕСЛИ ЕСТЬ ВИДЕО, НАДО ПОСМОТРЕТЬ ,ВЫПОЛНИТЬ ПО НЕМУ ЗАПИСИ, МНОГО НЕ НУЖНО ПИСАТЬ. Материала может быть выложено много, но это не значит, что всё надо записывать! После этого, сфотографируйте и отошлите мне на почту rimma.lu@gmail.com . Тетрадь привезете, когда перейдем на очную форму обучения.)Справа находится АХИВ БЛОГА , смотрите дату и номер своей группы
моя почта : rimma.lu@gmail.com Жду ваши фотоотчеты!
ГРУППА 501 БИОЛОГИЯ 3,4
- Углеводы, или сахариды, — одна из основных групп органических соединений. Они входят в состав клеток всех живых организмов.Основная функция углеводов — энергетическая (при расщеплении и окислении молекул углеводов выделяется энергия, которая обеспечивает жизнедеятельность организма). При избытке углеводов они накапливаются в клетке в качестве запасных веществ (крахмал, гликоген) и при необходимости используются организмом в качестве источника энергии. Углеводы также используются и в качестве строительного материала.Общая формула углеводов:
Cn(H2O)m .Углеводы состоят из углерода, водорода и кислорода. В состав производных углеводов могут входить и другие элементы.
В состав производных углеводов могут входить и другие элементы. Растворимые в воде углеводы. Моносахариды и дисахаридыПример:из моносахаридов наибольшее значение для живых организмов имеют рибоза, дезоксирибоза, глюкоза, фруктоза, галактоза.Глюкоза — основной источник энергии для клеточного дыхания.Фруктоза — составная часть нектара цветов и фруктовых соков.Рибоза и дезоксирибоза — структурные элементы нуклеотидов, являющихся мономерами нуклеиновых кислот (РНК и ДНК).
Растворимые в воде углеводы. Моносахариды и дисахаридыПример:из моносахаридов наибольшее значение для живых организмов имеют рибоза, дезоксирибоза, глюкоза, фруктоза, галактоза.Глюкоза — основной источник энергии для клеточного дыхания.Фруктоза — составная часть нектара цветов и фруктовых соков.Рибоза и дезоксирибоза — структурные элементы нуклеотидов, являющихся мономерами нуклеиновых кислот (РНК и ДНК).
Дисахариды образуются путём соединения двух молекул моносахаридов и по своим свойствам близки к моносахаридам. Например, и те и другие хорошо растворимы в воде и имеют сладкий вкус.Пример:сахароза (тростниковый сахар), мальтоза (солодовый сахар), лактоза (молочный сахар) — дисахариды, образовавшиеся в результате слияния двух молекул моносахаридов:сахароза (глюкоза+ фруктоза) — основной продукт фотосинтеза, транспортируемый в растениях.Лактоза (глюкоза+ галактоза) — входит в состав молока млекопитающих.Мальтоза (глюкоза+ глюкоза) — источник энергии в прорастающих семенах.Функции растворимых углеводов: транспортная, защитная, сигнальная, энергетическая.Нерастворимые в воде полисахаридыПолисахариды состоят из большого числа моносахаридов. С увеличением количества мономеров растворимость полисахаридов уменьшается и сладкий вкус исчезает.Пример:полимерные углеводы: крахмал, гликоген, целлюлоза, хитин.Функции полимерных углеводов: структурная, запасающая, энергетическая, защитная.
Крахмал состоит из разветвлённых спирализованных молекул, образующих запасные вещества в тканях растений.Целлюлоза является важным структурным компонентом клеточных стенок грибов и растений.Целлюлоза нерастворима в воде и обладает высокой прочностью.Хитин состоит из аминопроизводных глюкозы, входит в состав клеточных стенок некоторых грибов и формирует наружный скелет членистоногих животных.
Гликоген — резервный углевод животной клетки.В состав соединительных тканей животных входят сложные полисахариды. Они содержатся в межклеточном веществе кожи, в хрящах и сухожилиях. - Липиды — обширная группа жироподобных веществ (сложных эфиров жирных кислот и трёхатомного спирта глицерина), нерастворимых в воде. К липидам относят жиры, воски, фосфолипиды и стероиды (липиды, не содержащие жирных кислот).Липиды состоят из атомов водорода, кислорода и углерода.
 Липиды присутствуют во всех без исключения клетках, но их содержание в разных клетках сильно варьирует (от
Липиды присутствуют во всех без исключения клетках, но их содержание в разных клетках сильно варьирует (от2 –3 до50 –90 %).Липиды могут образовывать сложные соединения с веществами других классов, например с белками (липопротеины) и с углеводами (гликолипиды).Функции липидов:- запасающая — жиры являются основной формой запасания липидов в клетке.
- Энергетическая — половина энергии, потребляемой клетками позвоночных животных в состоянии покоя, образуется в результате окисления жиров (при окислении они дают более чем в два раза больше энергии по сравнению с углеводами).
- Жиры используются и как источник воды (при окислении
1 г жира образуется более1 г воды). - Защитная — подкожный жировой слой защищает организм от механических повреждений.
- Структурная — фосфолипиды входят в состав клеточных мембран.
- Теплоизоляционная — подкожный жир помогает сохранить тепло.
- Электроизоляционная — миелин, выделяемый клетками Шванна (образуют оболочки нервных волокон), изолирует некоторые нейроны, что во много раз ускоряет передачу нервных импульсов.
- Гормональная (регуляторная) — гормон надпочечников (кортизон) и половые гормоны (прогестерон и тестостерон) являются стероидами.
- Смазывающая — воски покрывают кожу, шерсть, перья и предохраняют их от воды. Восковым налётом покрыты листья многих растений, воск используется при строительстве пчелиных сот.
- ТЕМА 4: Белки.
- Белки (протеины, полипептиды) — самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. В состав молекул белков входят атомы углерода, кислорода, водорода, азота и иногда серы, фосфора и железа.Мономерами белков являются аминокислоты, которые (имея в своём составе карбоксильную и аминогруппы) обладают свойствами кислоты и основания (амфотерны).
 Благодаря этому аминокислоты могут соединяться друг с другом (их количество в одной молекуле может достигать нескольких сотен). В связи с этим молекулы белков имеют большие размеры, и их называют макромолекулами.
Благодаря этому аминокислоты могут соединяться друг с другом (их количество в одной молекуле может достигать нескольких сотен). В связи с этим молекулы белков имеют большие размеры, и их называют макромолекулами. Структура белковой молекулыПод структурой белковой молекулы понимают её аминокислотный состав, последовательность мономеров и степень скрученности молекулы белка.В молекулах белков встречается всего
Структура белковой молекулыПод структурой белковой молекулы понимают её аминокислотный состав, последовательность мономеров и степень скрученности молекулы белка.В молекулах белков встречается всего20 видов различных аминокислот, и огромное разнообразие белков создаётся за счёт различного их сочетания.- Последовательность аминокислот в составе полипептидной цепи — это первичная структура белка. Она уникальна для любого типа белка и определяет форму его молекулы, его свойства и функции.
- Длинная молекула белка сворачивается и приобретает сначала вид спирали в результате образования водородных связей между —СО и —NН группами разных аминокислотных остатков полипептидной цепи (между углеродом карбоксильной группы одной аминокислоты и азотом аминогруппы другой аминокислоты). Эта спираль — вторичная структура белка.
- Третичная структура белка — трёхмерная пространственная «упаковка» полипептидной цепи в виде глобулы (шарика). Прочность третичной структуры обеспечивается разнообразными связями, возникающими между радикалами аминокислот (гидрофобными, водородными, ионными и дисульфидными S–S связями).
- Некоторые белки (например, гемоглобин крови человека) имеют четвертичную структуру. Она возникает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс. Четвертичная структура удерживается непрочными ионными, водородными и гидрофобными связями.
 Структура белков может нарушаться (подвергаться денатурации) при нагревании, обработке некоторыми химическими веществами, облучении и др. При слабом воздействии распадается только четвертичная структура, при более сильном — третичная, а затем — вторичная, и белок остаётся в виде полипептидной цепи. В результате денатурации белок теряет способность выполнять свою функцию.Нарушение четвертичной, третичной и вторичной структур обратимо. Этот процесс называют ренатурацией.
Структура белков может нарушаться (подвергаться денатурации) при нагревании, обработке некоторыми химическими веществами, облучении и др. При слабом воздействии распадается только четвертичная структура, при более сильном — третичная, а затем — вторичная, и белок остаётся в виде полипептидной цепи. В результате денатурации белок теряет способность выполнять свою функцию.Нарушение четвертичной, третичной и вторичной структур обратимо. Этот процесс называют ренатурацией. Разрушение первичной структуры необратимо.Кроме простых белков, состоящих только из аминокислот, есть ещё и сложные белки, в состав которых могут входить углеводы (гликопротеины), жиры (липопротеины), нуклеиновые кислоты (нуклеопротеины) и др.Функции белков
Разрушение первичной структуры необратимо.Кроме простых белков, состоящих только из аминокислот, есть ещё и сложные белки, в состав которых могут входить углеводы (гликопротеины), жиры (липопротеины), нуклеиновые кислоты (нуклеопротеины) и др.Функции белков- Каталитическая (ферментативная) функция. Специальные белки — ферменты — способны ускорять биохимические реакции в клетке в десятки и сотни миллионов раз. Каждый фермент ускоряет одну и только одну реакцию. В состав ферментов входят витамины.

- Структурная (строительная) функция — одна из основных функций белков (белки входят в состав клеточных мембран; белок кератин образует волосы и ногти; белки коллаген и эластин — хрящи и сухожилия).

- Транспортная функция — белки обеспечивают активный транспорт ионов через клеточные мембраны (транспортные белки в наружной мембране клеток), транспорт кислорода и углекислого газа (гемоглобин крови и миоглобин в мышцах), транспорт жирных кислот (белки сыворотки крови способствуют переносу липидов и жирных кислот, различных биологически активных веществ).

- Сигнальная функция. Приём сигналов из внешней среды и передача информации в клетку происходит за счёт встроенных в мембрану белков, способных изменять свою третичную структуру в ответ на действие факторов внешней среды.
- Сократительная (двигательная) функция — обеспечивается сократительными белками — актином и миозином (благодаря сократительным белкам двигаются реснички и жгутики у простейших, перемещаются хромосомы при делении клетки, сокращаются мышцы у многоклеточных, совершенствуются другие виды движения у живых организмов).

- Защитная функция — антитела обеспечивают иммунную защиту организма; фибриноген и фибрин защищают организм от кровопотерь, образуя тромб.

- Регуляторная функция присуща белкам — гормонам (не все гормоны являются белками!). Они поддерживают постоянные концентрации веществ в крови и клетках, участвуют в росте, размножении и других жизненно важных процессах (например, инсулин регулирует содержание сахара в крови).
- Энергетическая функция — при длительном голодании белки могут использоваться в качестве дополнительного источника энергии после того, как израсходованы углеводы и жиры (при полном расщеплении
1 г белка до конечных продуктов выделяется17,6 кДж энергии). Аминокислоты, высвобождающиеся при расщеплении белковых молекул, используются для построения новых белков.

ГРУППА 408 ХИМИЯ 11,12
ТЕМА11: Получение и применение карбоновых кислот.
Получение карбоновых кислот I. В промышленности 1. Выделяют из природных продуктов (жиров, восков, эфирных и растительных масел) 2. Окисление алканов: 2CH4 + + 3O2 t,kat → 2HCOOH + 2H2O метан муравьиная кислота 2CH3-CH2-CH2-CH3 + 5O2 t,kat,p → 4CH3COOH + 2H2O н-бутан уксусная кислота 3. Окисление алкенов: CH2=CH2 + O2 t,kat → CH3COOH этилен СH3-CH=CH2 + 4[O] t,kat → CH3COOH + HCOOH (уксусная кислота+муравьиная кислота) 4. Окисление гомологов бензола (получение бензойной кислоты): C6H5-CnH2n+1 + 3n[O] KMnO4,H+→ C6H5-COOH + (n-1)CO2 + nH2O 5C6H5-CH3 + 6KMnO4 + 9H2SO4 → 5C6H5-COOH + 3K2SO4 + 6MnSO4 + 14H2O толуол бензойная кислота 5. Получение муравьиной кислоты: 1 стадия: CO + NaOH t,p → HCOONa (формиат натрия – соль) 2 стадия: HCOONa + H2SO4 → HCOOH + NaHSO4 6. Получение уксусной кислоты: CH3OH + CO t,p → CH3COOH Метанол II. В лаборатории 1. Гидролиз сложных эфиров: 2. Из солей карбоновых кислот: R-COONa + HCl → R-COOH + NaCl 3. Растворением ангидридов карбоновых кислот в воде: (R-CO)2O + H2O → 2 R-COOH 4. Щелочной гидролиз галоген производных карбоновых кислот: III. Общие способы получения карбоновых кислот 1. Окисление альдегидов: R-COH + [O] → R-COOH Например, реакция «Серебряного зеркала» или окисление гидроксидом меди (II) – качественные реакции альдегидов 2. Окисление спиртов: R-CH2-OH + 2[O] t,kat → R-COOH + H2O 3. Гидролиз галогензамещённых углеводородов, содержащих три атома галогена у одного атома углерода. 4. Из цианидов (нитрилов) – способ позволяет наращивать углеродную цепь: СH3-Br + Na-C≡N → CH3-CN + NaBr CH3-CN - метилцианид ( нитрил уксусной кислоты) СH3-CN + 2H2O t → CH3COONH4 ацетат аммония CH3COONH4 + HCl → CH3COOH + NH4Cl 5. Использование реактива Гриньяра R-MgBr + CO2 → R-COO-MgBr H2O → R-COOH + Mg(OH)Br ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ Муравьиная кислота – в медицине - муравьиный спирт (1,25% спиртовой раствор муравьиной кислоты), в пчеловодстве, в органическом синтезе, при получении растворителей и консервантов; в качестве сильного восстановителя. Уксусная кислота – в пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров). В домашнем хозяйстве как вкусовое и консервирующее вещество. Масляная кислота – для получения ароматизирующих добавок, пластификаторов и флотореагентов. Щавелевая кислота – в металлургической промышленности (удаление окалины). Стеариновая C17H35COOH и пальмитиновая кислота C15H31COOH – в качестве поверхностно-активных веществ, смазочных материалов в металлообработке. Олеиновая кислота C17H33COOH – флотореагент и собиратель при обогащении руд цветных металлов. ВИДЕО: Взаимодействие бромной воды с олеиновой кислотой СН2=СН-СООН + HCl → СН2Сl-СН2-СООН СН2=СН-СООН + Н2O → НО-СН2-СН2-СООН Две последние реакции протекают против правила Марковникова. Непредельные карбоновые кислоты и их производные способны к реакциям полимеризации. |
ТЕМА12: Краткие сведения о непредельных карбоновых кислотах.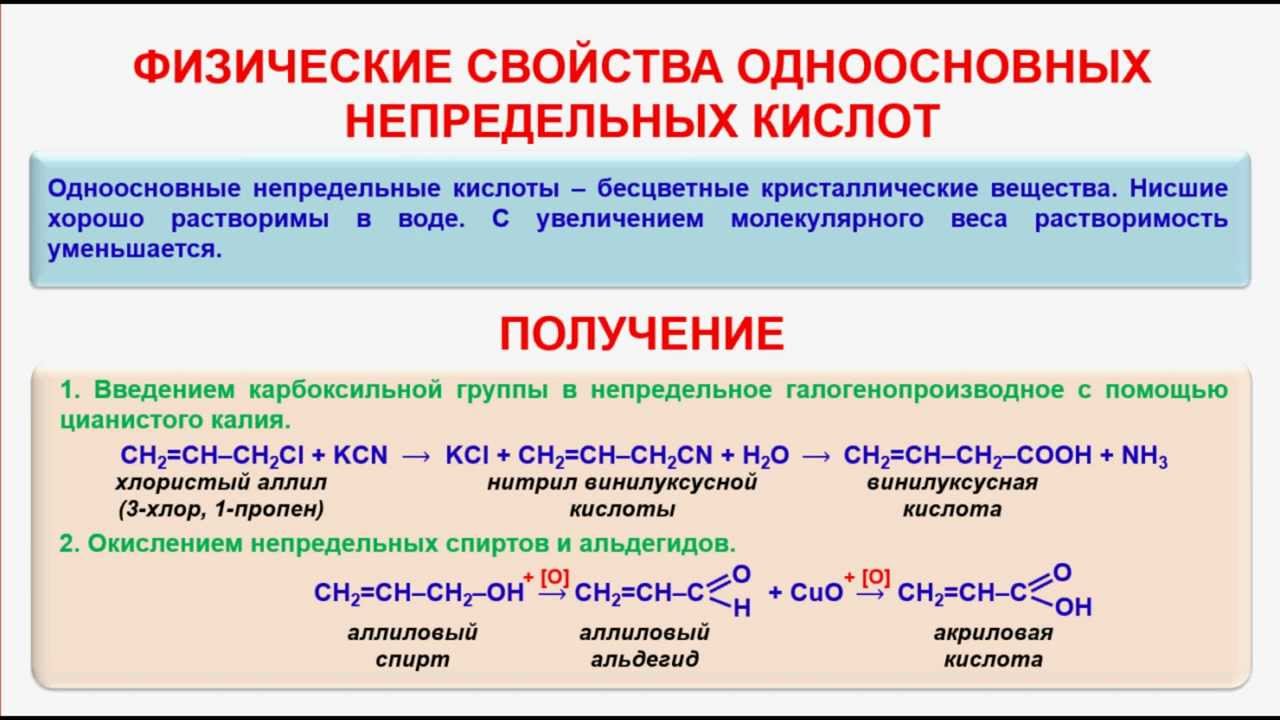
Подобно тому. как от формул предельных углеводородов можно вывести формулы непредельных углеводородов, от формул предельных карбоновых кислот можно вывести формулы непредельных карбоновых кислот. Одноосновные непредельные кислоты - производные ненасыщенных углеводородов, у которых один атом водорода замещен карбоксильной группой.
Номенклатура, изомерия.
В группе непредельных кислот наиболее часто используют эмпирические названия:
СН2=СН-СООН - акриловая (пропеновая) кислота,
СН2=С(СН3)-СООН - метакриловая (2-метилпропеновая) кислота.
Изомерия в группе непредельных одноосновных кислот связана с:
а) изомерией углеродного скелета;
б) положением двойной связи;
в) цис-транс-изомерией.
ГРУППА 406 ХИМИЯ 1
ТЕМА : Химические свойства металлов. |
В настоящее время известно
Некоторые металлы, такие как золото, серебро, ртуть, медь, олово, железо, свинец известны человечеству с глубокой древности. Алхимики связывали их с планетами и соответствующим образом обозначали: золото — Солнце, серебро — Луна, ртуть — Меркурий, медь — Венера, олово — Юпитер, свинец — Сатурн.

Рис. 1. Обозначение химических элементов в алхимии
У атомов наиболее типичных металлов, к которым относятся щелочные и щёлочноземельные, а также у переходных металлов на внешнем уровне содержится
Металлические свойства обусловлены способностью атомов отдавать электроны внешнего уровня. С ростом заряда ядра атома металлические свойства ослабевают слева направо по периоду и возрастают сверху вниз по подгруппе.
Отдавая электроны внешнего уровня, атомы металлов образуют устойчивую оболочку ближайшего благородного газа и приобретают положительную степень окисления.
химические элементы, атомы которых легко отдают электроны внешнего электронного слоя, превращаясь в положительные ионы.
Принципиальное отличие простых веществ металлов от простых веществ неметаллов заключается в том, что в химических реакциях металлы являются только восстановителями.
Наиболее распространённым в земной коре металлом является алюминий (
Для простых веществ металлов характерна металлическая кристаллическая решётка. В узлах металлической решётки находятся катионы металла, между которыми перемещаются электроны, образуя так называемый «электронный газ». «Электронный газ» движется между узлами решётки, обеспечивая её устойчивость. Металлическая решётка характерна для металлов и их сплавов. Свободно перемещающиеся электроны обусловливают характерные свойства веществ с металлической решёткой.

Рис. 2. Металлическая кристаллическая решётка
Металлическая связь и строение кристаллических решеток металлов обусловливают все важнейшие характерные физические свойства металлов, а именно: электропроводность, теплопроводность, пластичность, металлический блеск.
Электропроводность большинства металлов обусловлена присутствием в их кристаллических решётках подвижных электронов, которые направленно перемещаются под действием электрического поля. Наиболее электропроводными металлами являются серебро и медь, наименее — ртуть.
Теплопроводность металлов также связана с высокой подвижностью свободных электронов: сталкиваясь с колеблющимися в узлах решетки ионами, электроны обмениваются с ними энергией.
Пластичность – свойство вещества изменять форму под внешним воздействием и сохранять принятую форму после прекращения этого воздействия. Пластичность металлов обусловлена способностью их атомов под внешним воздействием смещаться друг относительно друга, но не рассыпаться за счёт прочного удерживания атомов общим электронным облаком. Наиболее пластичны золото, серебро, медь, олово. Так, золото легко прокатывают в тонкую фольгу, получая так называемое сусальное золото, которое используется в декоративных целях для золочения различных изделий.
Металлический блеск металлов обусловлен их способностью отражать световые лучи.
Такие свойства металлов, как твёрдость, плотность, температура плавления изменяются в широких пределах.
Наибольшей твёрдостью обладают металлы побочной подгруппы
Металлы с плотностью меньше

Рис. 3. Плотность некоторых металлов
При обычных условиях все металлы, кроме ртути имеют твёрдое агрегатное состояние. Ртуть — единственный жидкий металл. К легкоплавким металлам относятся цезий и галлий, они могут плавиться на ладони руки. Самый тугоплавкий металл — вольфрам.

Рис. 4. Температура плавления некоторых металлов
Металлы делят на чёрные, к которым относятся железо и его сплавы, и цветные — все остальные. Однако для большинства металлов характерен белый или серый цвет. Золото окрашено в жёлтый цвет, а медь — в красный. Золото, серебро, платину и некоторые другие металлы относят к драгоценным металлам.
 Коротко о главном
Коротко о главном
Наиболее распространённым в земной коре металлом является алюминий.
Металлы — химические элементы, атомы которых легко отдают электроны внешнего электронного слоя, превращаясь в положительные ионы.
Атомы большинства металлов содержат на внешнем уровне содержится
В химических реакциях металлы являются только восстановителями.
Важнейшими характерными физическими свойствами металлов являются высокие электро- и теплопроводность, пластичность, металлический блеск. Общие свойства металлов обусловлены металлической связью и строением их кристаллических решёток.
Такие свойства металлов, как твёрдость, плотность, температура плавления изменяются в широких пределах.
 Вопросы для самоконтроля
Вопросы для самоконтроля
- Сравните строение атомов металлов и неметаллов.
- Поясните, почему атомы металлов способны проявлять только восстановительные свойства
- Как изменяются металлические свойства в периодах и главных подгруппах с ростом заряда ядра атома?
- Какой тип кристаллической решетки характерен для металлов? Как свойства металлов связаны с особенностями их кристаллической решётки?
ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ
Химические свойства металлов определяются их активностью.
Простые вещества – металлы в химических реакциях всегда
являются восстановителями. Положение металла в ряду
активности характеризует то, насколько активно данный металл
способен вступать в химические реакции (т. е. то, насколько сильно
у него проявляются восстановительные свойства).
Среди металлов традиционно выделяют несколько групп.
Входящие в их состав представители характеризуются отличной от
других металлов химической активностью. Такими группами являются:
благородные металлы (серебро, золото, платина, иридий);
щелочные металлы – I(A) группа;
щелочноземельные металлы – II(A) группа, кроме Be, Mg.Металлы вступают в реакции с простыми веществами – неметаллами (кислород, галогены, сера, азот, фосфор и др.) и сложными веществами (вода, кислоты, растворы солей)
Взаимодействие с простыми веществами-неметаллами
1. Металлы взаимодействуют с кислородом, образуя оксиды:
4Li + O2 =обыч. усл.= 2Li2O
2Mg + O2 =t, °C= 2MgO
Серебро, золото и платина с кислородом не реагируют
Au + O2 ≠
Видео «Горение магния на воздухе»
Видео "Самовоспламенение никеля на воздухе"
2. Металлы взаимодействуют с галогенами (фтором, хлором, бромом и йодом), образуя галогениды – Ме+nГ-1n
2Na + Cl2 = 2NaCl
2Al + 3Cl2 = 2AlCl3
3. Металлы взаимодействуют с серой, образуя сульфиды.
Zn + S = ZnS
Видео «Взаимодействие цинка с серой»
4. Активные металлы при нагревании реагируют с азотом, фосфором и некоторыми другими неметаллами.
3Ca + N2 =t, °C= Ca3N2
3Na + P =t, °C= Na3P
Взаимодействие со сложными веществами
I. Взаимодействие воды с металлами
1). Взаимодействие с самыми активными металлами, находящимися в периодической системе в I(А) и II(А) группах (щелочные и щелочноземельные металлы) и алюминий. В результате образуются основание и газ водород.
Me + H2O = Me(OH)n + H2 (р. замещения)
Видео «Взаимодействие натрия с водой»
Внимание! Алюминий и магний ведут себя также:
2Al + 6H2O = 2Al(OH)3+3H2
Магний (в горячей воде):
Mg + 2H2O =t°C= Mg(OH)2+H2
2) Взаимодействие с менее активными металлами, которые расположены в ряду активности от алюминия до водорода.
Металлы средней активности, стоящие в ряду активности до (Н2) – Be, Fe, Pb, Cr, Ni, Mn, Zn – реагируют с образованием оксида металла и водорода
Me + Н2О = МехОу + Н2 (р. замещения)
Бериллий с водой образует амфотерный оксид:
Be + H2O =t°C= BeO + H2
Раскалённое железо реагирует с водяным паром, образуя смешанный оксид — железную окалину Fe3O4 и водород:
3Fe + 4H2O =t°C= FeO‧Fe2O3 + 4H2
3) Металлы, стоящие в ряду активности после водорода, не реагируют с водой.
Cu + H2O ≠ нет реакции
II. Взаимодействие растворов кислот с металлами
Металлы, стоящие в ряду активности металлов левее водорода, взаимодействуют с растворами кислот (раствор азотной кислоты – исключение), образуя соль и водород.
Кислота (раствор) + Me до (Н2) = Соль + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
Cu + H2SO4 ≠
Au + H2SO4 ≠
Видео «Электрохимический ряд напряжений - вытеснение водорода металлами»
III. Взаимодействие кислот-окислителей с металлами
Металлы особо реагируют с серной концентрированной и азотной кислотами:
H2SO4 (конц.) + Me = Сульфат + H2O + Х
2H2SO4 (конц.) + Cu =t°C= CuSO4 + 2H2O + SO2↑
8Na0 + 5H2+6SO4 = 4Na2+1SO4 + H2S-2↑ + 4H2O
Повторите «Окислительные свойства концентрированной серной кислоты»
HNO3 + Me = Нитрат + H2O + Х
4HNO3 (k) + Cu = Cu(NO3)2 + 4H2O + 2NO2↑
8HNO3 (p) + 3Cu = 3Cu(NO3)2 + 4H2O + 2NO↑
4Zn + 10HNO3 (раствор горячий) =t˚C= 4Zn(NO3)2 + N2O + 5H2O
4Zn + 10HNO3 (оч. разб. горячий) =t˚C= 4Zn(NO3)2 + NH4NO3 + 3H2O
Zn + 4HNO3 (конц. горячий) =t˚C= Zn(NO3)2 + 2NO2 + 2H2O
Повторите «Специфические свойства азотной кислоты»
IV. С растворами солей менее активных металлов
Ме + Соль = Новый металл + Новая соль
Fe + CuCl2 = FeCl2 + Cu
FeCl2 + Cu ≠
Видео «Электрохимический ряд напряжений металлов. Вытеснение металла из соли другими металлами»
Видео «Взаимодействие металлов с солями»
Активность металла в реакциях с кислотами, водными растворами солей и др. можно определить, используя электрохимический ряд, предложенный в 1865 г русским учёным Н. Н. Бекетовым: от калия к золоту восстановительная способность (способность отдавать электроны) уменьшается, все металлы, стоящие в ряду левее водорода, могут вытеснять его из растворов кислот; медь, серебро, ртуть, платина, золото, расположенные правее, не вытесняют водород.
Видео «Взаимодействие хлорида олова (II) с цинком («Оловянный ежик»)»
ГРУППА 405 ЭКОЛОГИЯ 3,4



