20.10.22 г. ЧЕТВЕРГ. 508, 405,303
Здравствуйте, уважаемые студенты, записывайте дату, тему и выполняйте необходимые записи (ВСЁ подряд не пишите, читайте, выбирайте, можно составить план, ЕСЛИ ЕСТЬ ВИДЕО, НАДО ПОСМОТРЕТЬ ,ВЫПОЛНИТЬ ПО НЕМУ ЗАПИСИ, МНОГО НЕ НУЖНО ПИСАТЬ. Материала может быть выложено много, но это не значит, что всё надо записывать! После этого, сфотографируйте и отошлите мне на почту rimma.lu@gmail.com . Тетрадь привезете, когда перейдем на очную форму обучения.)
Справа находится АХИВ БЛОГА , смотрите дату и номер своей группы
моя почта : rimma.lu@gmail.com Жду ваши фотоотчеты!
ГРУППА 508 БИОЛОГИЯ 8,9
ТЕМА 8: АТФ и другие органические соединения клетки.
Универсальным источником энергии во всех клетках служит


Нуклеотиды могут также принимать участие в регуляции окислительных процессов в клетке.
Витамины принимают участие в обмене веществ преимущественно как составная часть сложных ферментов. Их отсутствие или недостаток приводит к тяжёлым нарушениям жизнедеятельности организма.
ТЕМА 9:Клетка – элементарная единица живого.
Клетка - элементарная единица структурной организации живой материи
Клетка — элементарная единица структуры, функции и развития живой материи, которая характеризуется подразделением на ядро (или нуклеоид), цитоплазму и клеточную мембрану и обладает всем комплексом свойств живого: самовоспроизведением, саморазвитием, ростом, саморегуляцией, обменом веществ и энергии, раздражимостью, подвижностью, адаптацией и способностью противостоять энтропии.
В состав многоклеточных организмов наряду с клетками входят симпласты, синцитии1 и межклеточное вещество. Однако ведущей формой структурной организации организмов, безусловно, является клетка, поскольку все перечисленные выше формы являются либо производными клетки (клеток), либо образуются в результате ее синтетической деятельности.
Все клеточные формы органического мира, как указывалось выше, подразделяются на прокариот и эукариот; их сравнительная характеристика представлена в табл. 3.1 и на рис. 3.1.
Таблица 3.1
Сравнительная характеристика прокариот и эукариот
Признаки и свойства | Прокариоты | Эукариоты |
Морфологически оформленное ядро | Отсутствует | Имеется |
Нуклеоид* | И меется | Отсутствует |
Форма молекулы ДНК | Кольцевая | Линейная |
Длина ДНК | 1 (условно) | 1000 (по отношению к прокариотам) |
Ядерные белки, связанные с ДНК | Отсутствуют | Имеются |
CRISPR-систсма в геноме** | Имеется | Отсутствует |
Плоидность генома | Гаплоидный | Диплоидный*** |
Фенотипические проявления мутаций | Каждая мутация реализуется в фенотипе | Возможно сохранение мутантного рецессивного гена в гетерозиготном состоянии |
Микротрубочки и состоящие из них структуры (цеитриоли и др.) | Отсутствуют | Имеются |
Деление митозом | Не характерно**** | Характерно |
Клеточная оболочка | Плазмалемма + клеточная стенка (из пептидоглика- нов) | Плазмалемма (+ клеточная стенка из целлюлозы у растений и хитина — у грибов) |
Сократительные белки (актин и миозин) | Отсутствуют | Имеются |
1 Симпласты и синцитии состоят из единой цитоплазмы с множеством ядер и покрыты клеточной мембраной. Симпласты образуются в результате слияния нескольких клеток (скелетное мышечное волокно), синцитии — в результате многократного митотического деления ядра без последующего разделения клеточного тела (часть сперматогенного эпителия).
Признаки и свойства | Прокариоты | Эукариоты |
Жгутики | Пить жгхтика построена из субъединиц белка флагсл- лина, образующих спираль | Каждый жгутик содержит набор микротрубочек, собранных в группы |
Способ питания | Голофитный (всасывание растворенных веществ; не способны к образованию псевдоподий) | Голозойный (захват твердых частиц) |
Система внутриклеточных мембран | Отсутствует (внутриклеточные потоки не упорядочены) | Имеется (внутриклеточные потоки упорядочены) |
Рибосомы | Имеются, масса небольшая | Имеются |
Митохондрии и хлоропласты | Отсутствуют | Имеются |
Локализация биоэнергетических структур | Клеточная оболочка | Митохондрии |
Эволюционные перспективы | Адаптивная эволюция (структурные перестройки невозможны) | 11рогрессивная (возможны глубокие структурные преобразования) |
* Находящаяся в центре прокариотической клетки структура, имеющая форму ромашки (центральная часть — остов — образован РНК, «лепестки» — около 50 петель ДНК).
** Особая генетическая конструкция, обеспечивающая иммунную защиту бактерий от вирусов и играющая определенную роль в рекомбинации и репарации ДНК.
*** За исключением половых клеток и соматических клеток некоторых водорослей, грибов, растений (мхов).
**** Прокариотические клетки размножаются простым поперечным делением.

Рис. 3.1. Общая схема строения прокариотической (я) и эукариотической (6) клеток:
1 — плазматическая мембрана; 2 — клеточная стенка; 3 — жгутик; 4 — нуклеоид; 5 — рибосомы; 6 — ядро; 7 — мембранные органеллы
Эукариоты в эволюционном плане оказались более перспективными по сравнению с прокариотами, так как:
- • содержали больший объем генетической информации (двойной набор генов, множество копий отдельных генов);
- • имели возможность накапливать в популяциях особей рецессивные мутантные гены в гетерозиготном состоянии и тем самым формировать резерв наследственной изменчивости (важное условие для эффективного протекания естественного отбора);
- • могли осуществлять более тонкую и сложную регуляцию жизнедеятельности клеток (множество регуляторных генов, возможность использовать геном по частям);
- • имели более совершенную пространственно-временную организацию метаболизма (благодаря компартментации внутреннего объема клетки, т.е. разделения пространства клетки мембранами на отсеки);
- • обладали более пластичной клеточной оболочкой, способной к образованию разнообразных межклеточных соединений с различными функциями (контактов);
- • имели высокосовершенный механизм воспроизведения генетически идентичных клеток (митоз), на базе которого при дальнейшей эволюции многоклеточных форм возник мейоз;
- • обладали более эффективным механизмом извлечения и аккумулирования энергии (дыхание).
ГРУППА 405 ХИМИЯ 21,22
ТЕМА 21,22:Алкены. Этилен, его получение (дегидрированием этана, деполимеризацией полиэтилена). Гомологический ряд, изомерия, номенклатура алкенов.
Непредельные углеводороды
К непредельным относят углеводороды, содержащие в молекулах кратные связи между атомами углерода. Непредельными являются алкены, алкины, алкадиены (полиены). Непредельным характером обладают также циклические углеводороды, содержащие двойную связь в цикле (циклоалкены), а также циклоалканы с небольшим числом атомов углерода в цикле (три или четыре атома). Свойство «непредельности» связано со способностью этих веществ вступать в реакции присоединения, прежде всего водорода, с образованием предельных, или насыщенных углеводородов — алканов.
Алкены
Алкены - непредельные (ненасыщенные) ациклические алифатические углеводороды, имеющие в молекуле одну двойную связь С=С. Такая связь содержит одну сигма-связь (σ-связь) и одну пи-связь (π-связь). Своё второе название — олефины — алкены получили по аналогии с жирными непредельными кислотами (олеиновая, линолевая), остатки которых входят в состав жидких жиров — масел.
Алкены также называют этиленовыми углеводородами, по первому члену гомологического ряда - этилену - CH2=CH2. Общая формула их гомологического ряда - CnH2n.
Гомологический ряд алкенов | Структурные формулы | Названия, суффикс ен, илен |
C2Н4 | CH2=CH2 | этен, этилен |
C3H6 | CH2=CH-CH3 | пропен |
C4H8 | CH2=CH-CH2-CH3 | бутен-1 |
CH3-CH=CH-CH3 | бутен-2 |
Гомологи
СH2=CH2 этен
 СH2=CH-CH3 пропен
СH2=CH-CH3 пропен
СH2=CH-CH2-CH3 бутен-1
СH2=CH-CH2-CH2-СН3 пентен-1
Физические свойства алкенов
Этилен (этен) – бесцветный газ с очень слабым сладковатым запахом, немного легче воздуха, малорастворим в воде.
С2 – С4 (газы)
С5 – С17 (жидкости)
С18 – (твёрдые)
§ Алкены не растворяются в воде, растворимы в органических растворителях (бензин, бензол и др.)
§ Легче воды
§ С увеличением Mr температуры плавления и кипения увеличиваются
Строение
Этилен
Характеристики и физические свойства этилена
Представляет собой бесцветный горючий газ (строение молекулы показано на рис. 1), который обладает слабым запахом. Плохо растворяется в воде, но хорошо в диэтиловом эфире и углеводородах.
Рис. 1. Строение молекулы этилена.
Таблица 1. Физические свойства этилена.
Молекулярная формула | CH2=CH2 (C2H4) |
Молярная масса, г/моль | 28 |
Плотность, г/см3 | 0,001178 |
Температура плавления, oС | -169,2 |
Температура кипения, oС | -103,7 |
Получение этилена
Способы получения этилена можно разделить на промышленные и лабораторные. В первом случае этен – это продуктдегидрирования этана, полученного при крекинге нефти.
В лабораторных условиях этилен можно получить при помощи дегидратации этанола (1), дегалогенированиямоно- и дигалогенпроизводных этана (2, 3) или при неполном гидрировании ацетилена (4):
CH3-CH2-OH→CH2=CH2 + H2O (H2SO4 (conc), to = 170) (1);
CH3-CH2-Br + NaOHalcohol→CH2=CH2 + NaBr + H2O (to) (2);
Cl-CH2-CH2-Cl + Zn(Mg) →CH2=CH2 + ZnCl2(MgCl2) (3);
CH≡CH + H2→CH2=CH2 (Pd, to) (4).
Запомните характеристики sр2 –гибридизации
1) Плоское тригональное (треугольное) строение
2) Угол – HCH - 120°
3) Длина (-С=С-) связи – 0,134 нм
4) Связи - σ, p
5) Невозможно вращение относительно (-С=С-) связи
Номенклатура
Названия алкенов формируются путем добавления суффикса "ен" к названию алкана с соответствующим числом: этен, пропен, бутен, пентен и т.д.
При составлении названия алкена важно учесть, что главная цепь атомов углерода должна обязательно содержать двойную связь. Принято начинать нумерацию атомов углерода с того края, к которому ближе двойная связь. В конце названия указывают атом углерода, у которого начинается двойная связь.
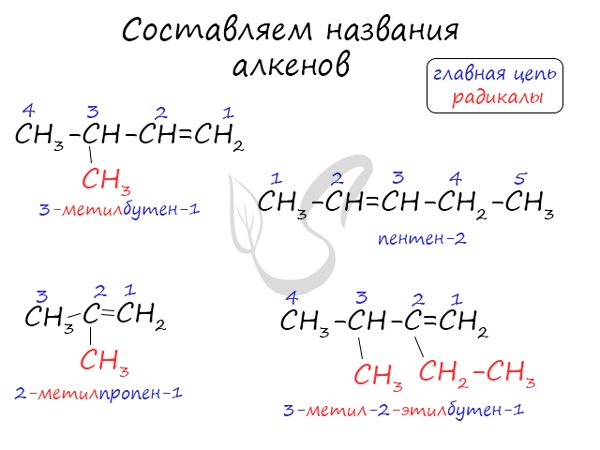
Образование названий алкенов по номенклатуре ИЮПАК
ТЕМА 22:Химические свойства этилена: горение, качественные реакции (обесцвечивание бромной воды и раствора перманганата калия), гидратация, полимеризация
Химические свойства этилена
Этилен способен присоединять водород (гидрирование) (5), галогены (галогенирование) (6), галогеноводороды (гидрогалогенирование) (7) и воду (гидратация) (8):
CH2=CH2 + H2→ CH3-CH3 (kat = Pt) (5);
CH2=CH2 + Br2→BrCH-CHBr (6);
CH2=CH2 + H-Cl → H2C-CHCl (7);
CH2=CH2 + H-OH → CH3-CH2-OH (H+, to) (8).
В зависимости от условий проведения реакции окисления этилена могут быть получены многоатомные спирты (9), эпоксиды (10) или альдегиды (11):
CH2=CH2 + 2KMnO4 + 2KOH → HO-CH2-CH2-OH + 2K2MnO4 (9);
2CH2=CH2 + O2 → 2C2OH4 (эпоксид) (kat = Ag,to) (10);
2CH2=CH2 + O2 → 2CH3-C(O)H (kat = PdCl2, CuCl) (11).
В результате горения этилена происходит разрыв всех связей в молекуле, а продуктами реакции являются углекислый газ и воды:
C2H4 + 2O2→ 2CO2 + 2H2O.
Этилен подвергается полимеризации:
nCH2=CH2→ -[-CH2-CH2-]-n (kat, to).
Кроме этого, если проводить галогенирование этилена при температуре 400oС, то разрыва двойной связи происходить не будет, будет замещаться один атом водорода в углеводородном радикале:
CH2=CH2 + Cl2→ CH2=CH-Cl + HCl.
Применение этилена
Основное направление использование этилена — промышленный органический синтез таких соединений как галогенопроизводные, спирты (этанол, этиленгликоль), уксусный альдегид, уксусная кислота и др. Кроме этого данное соединение в производстве полимеров.
| Задание | Осуществите ряд превращений: этан → этен → этанол → этен → хлорэтан → бутан. |
| Решение | Для получения этена из этана необходимо использовать реакцию дегидрирования этана, которая протекает в присутствии катализатора (Ni, Pd, Pt) и при нагревании: С2H6 →C2H4 + H2. Получение этанола из этена осуществляют по реакции гидратации, протекающей водой в присутствии минеральных кислот (серной, фосфорной): С2H4 + H2O = C2H5OH. Для получения этена из этанола используют реакцию дегидротации: C2H5OH →(t, H2SO4) → C2H4 + H2O. Получение хлорэтана из этена осуществляют по реакции гидрогалогенирования: С2H4 + HCl → C2H5Cl. Для получения бутана из хлорэтана используют реакцию Вюрца: 2C2H5Cl +2Na → C4H10 + 2NaCl. |
ГРУППА 405 экология 14
ТЕМА 14: ИСПОЛЬЗОВАНИЕ ОРУДИЙ И ЭНЕРГИИ.
ГРУППА 303 ЭКОЛОГИЯ 4,5
Тема:4 РОСТ ЧИСЛЕННОСТИ НАСЕЛЕНИЯ.
ОТКРОЙТЕ УЧЕБНИК ЭКОЛОГИИ (это ссылка на электронный учебник.) СТР. 205-205. ПАРАГРАФ 31. ПРОЧИТАЙТЕ, СОСТАВЬТЕ ПЛАН ОТВЕТА.РАССМОТРИТЕ РИСУНКИ. ПИСЬМЕННО ОТВЕТЬТЕ НА ВОПРОС ДИСКУССИИ.С.205
Тема:5 Самостоятельная работа
Письменно ответьте на вопросы(вопросы записывать)
1) с.201, вопрос 2
2)с. 205, вопрос 1