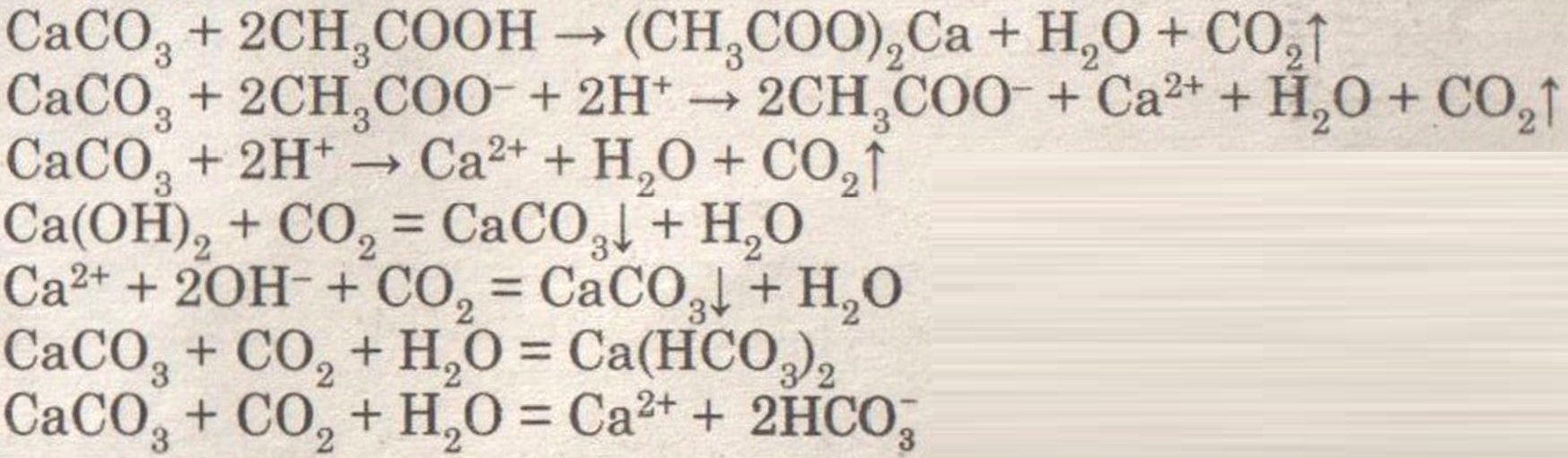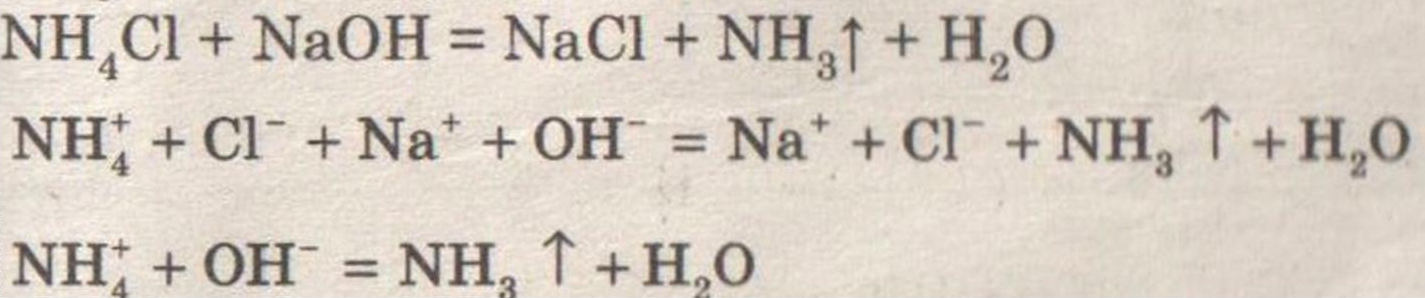17.11.22 г. ЧЕТВЕРГ. 306, 405, 303
Здравствуйте, уважаемые студенты, записывайте дату, тему и выполняйте необходимые записи (ВСЁ подряд не пишите, читайте, выбирайте, можно составить план, ЕСЛИ ЕСТЬ ВИДЕО, НАДО ПОСМОТРЕТЬ ,ВЫПОЛНИТЬ ПО НЕМУ ЗАПИСИ, МНОГО НЕ НУЖНО ПИСАТЬ. Материала может быть выложено много, но это не значит, что всё надо записывать! После этого, сфотографируйте и отошлите мне на почту rimma.lu@gmail.com . Тетрадь привезете, когда перейдем на очную форму обучения.)
Справа находится АХИВ БЛОГА , смотрите дату и номер своей группы
моя почта : rimma.lu@gmail.com Жду ваши фотоотчеты!
ГРУППА 306 БИОЛОГИЯ 13,14
ТЕМА 13,14: Обмен веществ.Фотосинтез.
ПРОЧИТАЙТЕ, РАССМОТРИТЕ РИСУНКИ, СОЗДАЙТЕ КРАТКИЙ КОНСПЕКТ,МОЖНО ЧЕРТИТЬ СХЕМЫ,ГДЕ ЭТО НАДО.
Обязательным условием существования любого организма является постоянный приток питательных веществ и постоянное выделение конечных продуктов химических реакций, происходящих в клетках. Клетка постоянно находится в движении – цитоплазма перемещается, увлекая за собой органоиды и включения, активно работают рибосомы и митохондрии, совершается множество химических превращений. Все живые организмы, существующие на Земле, представляют собой открытые системы, характеризующиеся способностью активно обмениваться с окружающей средой веществами и энергией. Из окружающей среды в клетку поступают различные вещества, а из клетки в окружающую среду удаляются ненужные продукты обмена – происходит обмен веществ, или метаболизм (Рис. 1).

Рис. 1. Обмен веществ клетки с окружающей средой (Источник)
Питательные вещества используются организмами в качестве источника атомов химических элементов (прежде всего атомов углерода), из которых строятся либо обновляются все структуры. В организм, кроме питательных веществ, поступают также вода, кислород, минеральные соли.
Поступившие в клетки органические вещества (или синтезированные в ходе фотосинтеза) расщепляются на строительные блоки – мономеры и направляются во все клетки организма (Рис. 2). Часть молекул этих веществ расходуется на синтез специфических органических веществ, присущих данному организму. В клетках синтезируются белки, липиды, углеводы, нуклеиновые кислоты и другие вещества, которые выполняют различные функции (строительную, каталитическую, регуляторную, защитную и так далее).
Другая часть низкомолекулярных органических соединений, поступивших в клетки, идет на образование АТФ, в молекулах которой заключена энергия, предназначенная непосредственно для выполнения работы.

Рис. 2. Распределение органических веществ
Энергия необходима для синтеза всех специфических веществ организма, поддержания его высокоупорядоченной организации, активного транспорта веществ внутри клеток, из одних клеток в другие, из одной части организма в другую, для передачи нервных импульсов, передвижения организмов, поддержания постоянной температуры тела (у птиц и млекопитающих) и для других целей.
Обмен веществ (метаболизм) – совокупность биохимических реакций, протекающих в клетке и обеспечивающих процессы ее жизнедеятельности.
В ходе превращения веществ в клетках образуются конечные продукты обмена, которые могут быть токсичными для организма и выводятся из него (например, аммиак). Таким образом, все живые организмы постоянно потребляют из окружающей среды определенные вещества, преобразуют их и выделяют в среду конечные продукты.
В зависимости от общей направленности процессов выделяют катаболизм и анаболизм.
Анаболизм (ассимиляция) – совокупность химических процессов, направленных на образование и обновление структурных частей клеток, этот процесс имеет второе название – пластический обмен.
Фотосинтез: 6Н2О + 6СО2 → С6Н12О6 + 6СО2 ↑
Сюда можно отнести, например, фиксацию азота и биосинтез белка, синтез углеводов из углекислого газа и воды в ходе фотосинтеза, синтез полисахаридов, липидов, нуклеотидов, ДНК, РНК и других веществ. Анаболизм является созидательным этапом обмена веществ, он всегда осуществляется с потреблением энергии и с участием ферментов.
Катаболизм (диссимиляция) – совокупность реакций, в которых происходит распад крупных органических молекул до простых соединений с одновременным высвобождением энергии.
Катаболизм обеспечивает энергией все процессы, протекающие в клетке, и имеет второе название – энергетический обмен.
Дыхание: С6Н12О6 + 6СО2 → 6Н2О + 6СО2 + АТФ
При разрыве химических связей молекул органические соединения энергии высвобождаются и запасаются главным образом в виде молекул аденозинтрифосфорной кислоты – АТФ, универсального источника энергии у всех живых организмов (Рис. 3).

Рис. 3. Строение молекулы АТФ
По своей химической природе АТФ является мононуклеотидом и состоит из азотистого основания аденина, углевода рибозы и трех остатков фосфорной кислоты, соединенных между собой макроэргическими связями. Выделение энергии в клетке происходит при отделении одного из фосфорных остатков от молекулы АТФ, разрыв этой связи высвобождает 7,3 килокалории, тогда как при разрыве химических связей других соединений энергии выделяется в три-четыре раза меньше. При этом образуется молекула аденозиндифосфата – АДФ, с двумя фосфорными остатками. Она легко может восстановиться до АТФ, присоединив один остаток фосфорной кислоты или отдать еще один фосфорный остаток и превратиться в аденозинмонофосфат – АМФ (Рис. 4).

Рис. 4. Выработка энергии в клетке
Переход АТФ в АДФ и обратно – это основной механизм выработки энергии в клетке. Отщепление от АТФ и АДФ фосфорного остатка приводит к выделению энергии, а присоединение к АМФ и АДФ фосфорного остатка приводит к накоплению энергии.
ТЕМА:ФОТОСИНТЕЗ.
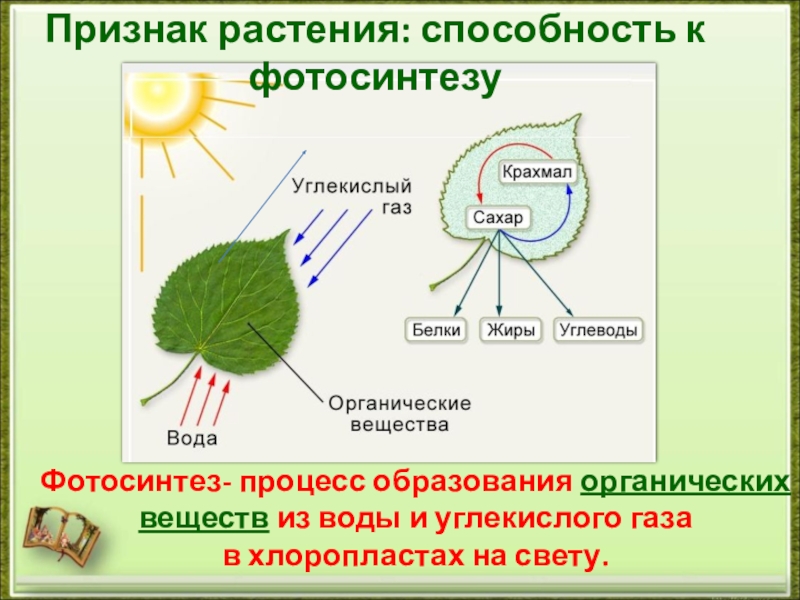
Фотосинтез – это процесс образования органических веществ в зелёных растениях. Фотосинтез создал всю массу растений на Земле и обогатил атмосферу кислородом.
КАК ПИТАЕТСЯ РАСТЕНИЕ?
Раньше люди были уверены, что все вещества для своего питания растения берут из почвы. Но один опыт показал, что это не так.
В горшок с землёй было посажено дерево. При этом измерили массу и земли, и дерева. Когда через несколько лет снова взвесили то и другое, оказалось, что масса земли уменьшилась всего на несколько граммов, а масса растения увеличилась на много килограмм.
В почву вносили только воду. Откуда же взялись эти килограммы растительной массы?
Из воздуха. Все органические вещества растений созданы из углекислого газа атмосферы и почвенной воды.
ЭНЕРГИЯ
Животные и человек питаются растениями, чтобы получить энергию для жизни. Эта энергия содержится в химических связях органических веществ. Откуда она там?
Известно, что растение не может нормально расти без света. Свет и является энергией, с помощью которой растение строит органические вещества своего тела.
Не важно какой это свет, солнечный или электрический. Любой луч света несёт энергию, которая становится энергией химический связей и как клей удерживает атомы в больших молекулах органических веществ.
ГДЕ ИДЁТ ФОТОСИНТЕЗ
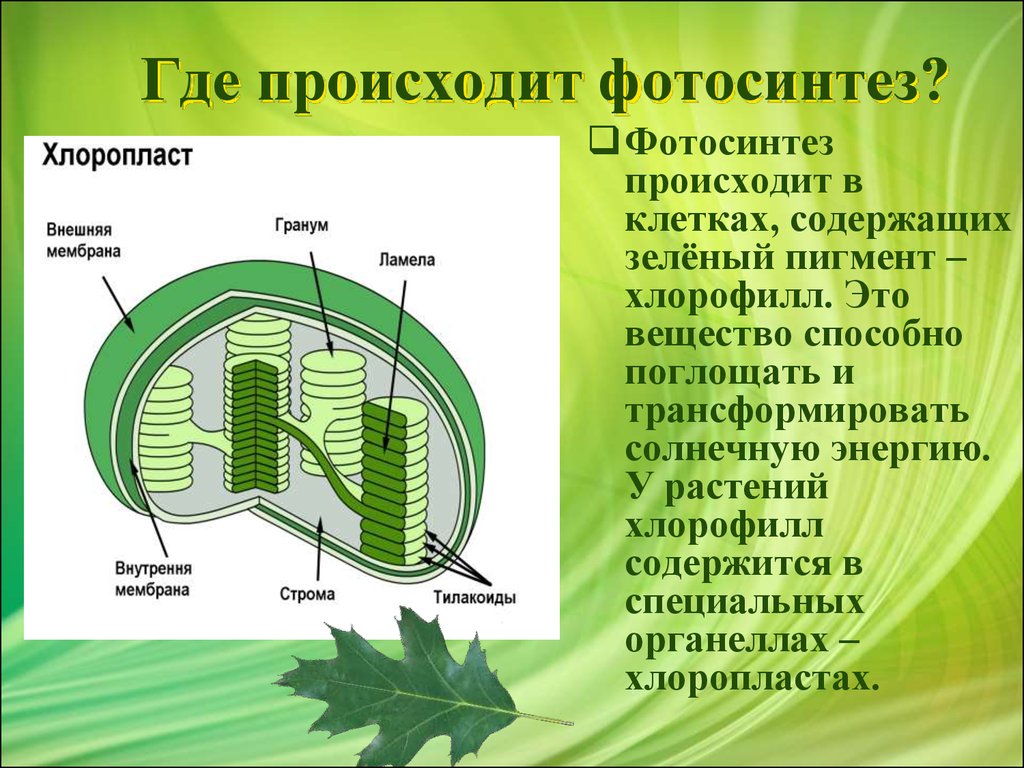
Фотосинтез проходит только в зелёных частях растений, а точнее, в особых органах растительных клеток – хлоропластах.

Хлоропласты являются разновидностью пластид. Они всегда зелёные, т. к. содержат вещество зелёного цвета – хлорофилл.
Хлоропласт отделён от остального объёма клетки мембраной и имеет вид зёрнышка. Внутреннее пространство хлоропласта называется стромой. В ней и начинаются процессы фотосинтеза.
Хлоропласты являются как бы фабрикой, на которую поступает сырьё:
- углекислый газ (формула – СО₂);
- вода (Н₂О).
Вода поступает из корней, а углекислый газ – из атмосферы через особые отверстия в листьях-устьица. Свет является энергией для работы фабрики, а полученные органические вещества – продукцией.
Сначала производятся углеводы (глюкоза), но впоследствии из них образуется множество веществ разнообразных запахов и вкусов, которые так любят животные и люди.
Из хлоропластов полученные вещества транспортируются в разные органы растения, где откладываются в запас, либо используются для процессов жизнедеятельности.
РЕАКЦИЯ ФОТОСИНТЕЗА
В общем виде уравнение фотосинтеза выглядит так:
СО₂(углекислый газ) + Н₂О(вода) = органические вещества(глюкоза) + О₂ (кислород)
Зелёные растения входят в группу автотрофов (в переводе – «сам питаюсь») – организмов, которым для получения энергии не нужны другие организмы.
Основная функция фотосинтеза – создание органических веществ, из которых строится тело растений.
Выделение кислорода – побочный эффект процесса.
ЗНАЧЕНИЕ ФОТОСИНТЕЗА
Роль фотосинтеза в природе чрезвычайно велика. Благодаря ему создан весь растительный мир и озоновый экран нашей планеты.
Благодаря фотосинтезу растения:
- являются источником кислорода для атмосферы;
- переводят энергию солнца в доступную для животных и человека форму.
Жизнь на Земле стала возможной при накоплении достаточного количества кислорода в атмосфере. Ни человек, ни животные не смогли бы жить в те далёкие времена, когда его не было, или было мало.
КАКАЯ НАУКА ИЗУЧАЕТ ПРОЦЕСС ФОТОСИНТЕЗА
Фотосинтез изучают разные науки, но больше всего ботаника и физиология растений.
Ботаника – это наука о растениях и, поэтому изучает его как важный жизненный процесс растений.
 Наиболее подробно изучает фотосинтез физиология растений. Учёные-физиологи определили, что этот процесс сложный и имеет стадии:
Наиболее подробно изучает фотосинтез физиология растений. Учёные-физиологи определили, что этот процесс сложный и имеет стадии:
- световую;
- темновую.
Это значит, что фотосинтез начинается на свету, но заканчивается в темноте.

ГРУППА 405 ЭКОЛОГИЯ 28,29
ТЕМА 28,29 : СОВРЕМЕННОЕ СОСТОЯНИЕ И ОХРАНА НЕДР.
ОТКРОЙТЕ УЧЕБНИК ЭКОЛОГИИ (это ссылка на электронный учебник.) ПАРАГРАФ 37- ЧИТАТЬ, СТР.253, ВОПРОС 1 ПИСЬМЕННО ОТВЕТИТЬ И ПРИСЛАТЬ.
ГРУППА 405 ХИМИЯ 35
ТЕМА 35 : Карбоновые кислоты. Понятие о карбоновых кислотах. Карбоксильная группа как функциональная. Гомологический ряд предельных однооснóвных карбоновых кислот. Получение карбоновых кислот окислением альдегидов.
Карбоновые кислоты - органические вещества, молекулы которых содержат одну или несколько карбоксильных групп.
Карбоксильная группа ![]() (сокращенно —COOH) - функциональная группа карбоновых кислот - состоит из карбонильной группы и связанной с ней гидроксильной группы.
(сокращенно —COOH) - функциональная группа карбоновых кислот - состоит из карбонильной группы и связанной с ней гидроксильной группы.
По числу карбоксильных групп карбоновые кислоты делятся на одноосновные, двухосновные и т.д.
Общая формула одноосновных карбоновых кислот R—COOH. Пример двухосновной кислоты - щавелевая кислота HOOC—COOH.
По типу радикала карбоновые кислоты делятся на предельные (например, уксусная кислота CH3COOH), непредельные [например, акриловая кислота
Изомеры и гомологи
Одноосновные предельные карбоновые кислоты R—COOH являются изомерами сложных эфиров ![]() (сокращенно R'—COOR'') с тем же числом атомов углерода. Общая формула и тех, и других CnH2nO2.
(сокращенно R'—COOR'') с тем же числом атомов углерода. Общая формула и тех, и других CnH2nO2.
| г о м о л о г и | HCOOH метановая (муравьиная) | ||||
| CH3COOH этановая (уксусная) | HCOOCH3 метиловый эфир муравьиной кислоты | ||||
| CH3CH2COOH пропановая (пропионовая) | HCOOCH2CH3 этиловый эфир муравьиной кислоты | CH3COOCH3 метиловый эфир уксусной кислоты | |||
бутановая (масляная) | 2-метилпропановая | HCOOCH2CH2CH3 пропиловый эфир муравьиной кислоты | CH3COOCH2CH3 этиловый эфир уксусной кислоты | CH3CH2COOCH3 метиловый эфир пропионовой кислоты | |
| и з о м е р ы | |||||
Алгоритм составления названий карбоновых кислот
- Найдите главную углеродную цепь - это самая длинная цепь атомов углерода, включающая атом углерода карбоксильной группы.
- Пронумеруйте атомы углерода в главной цепи, начиная с атома углерода карбоксильной группы.
- Назовите соединение по алгоритму для углеводородов.
- В конце названия допишите суффикс "-ов", окончание "-ая" и слово "кислота".
В молекулах карбоновых кислот p-электроны атомов кислорода гидроксильной группы взаимодействуют с электронами ![]() -связи карбонильной группы, в результате чего возрастает полярность связи O—H, упрочняется
-связи карбонильной группы, в результате чего возрастает полярность связи O—H, упрочняется ![]() -связь в карбонильной группе, уменьшается частичный заряд (
-связь в карбонильной группе, уменьшается частичный заряд (![]() +) на атоме углерода и увеличивается частичный заряд (
+) на атоме углерода и увеличивается частичный заряд (![]() +) на атоме водорода.
+) на атоме водорода.

Последнее способствует образованию прочных водородных связей между молекулами карбоновых кислот.
Физические свойства предельных одноосновных карбоновых кислот в значительной степени обусловлены наличием между молекулами прочных водородных связей (более прочных, чем между молекулами спиртов). Поэтому температуры кипения и растворимость в воде у кислот больше, чем у соответствующих спиртов.
Химические свойства кислот
Упрочнение ![]() -связи в карбонильной группе приводит к тому, что реакции присоединения для карбоновых кислот нехарактерны.
-связи в карбонильной группе приводит к тому, что реакции присоединения для карбоновых кислот нехарактерны.
- Горение:CH3COOH + 2O2
 2CO2 + 2H2O
2CO2 + 2H2O - Кислотные свойства.
Из-за высокой полярности связи O-H карбоновые кислоты в водном растворе заметно диссоциируют (точнее, обратимо с ней реагируют):HCOOH HCOO- + H+ (точнее HCOOH + H2O
HCOO- + H+ (точнее HCOOH + H2O  HCOO- + H3O+)
HCOO- + H3O+)
Все карбоновые кислоты - слабые электролиты. С увеличением числа атомов углерода сила кислот убывает (из-за снижения полярности связи O-H); напротив, введение атомов галогена в углеводородный радикал приводит к возрастанию силы кислоты. Так, в рядуHCOOH CH3COOH
CH3COOH  C2H5COOH
C2H5COOH
сила кислот снижается, а в рядуCH3COOH 
CH2ClCOOH 
CHCl2COOH 
CCl3COOH уксусная кислота монохлоруксусная кислота дихлоруксусная кислота трихлоруксусная кислота
- возрастает.
Карбоновые кислоты проявляют все свойства, присущие слабым кислотам:Mg + 2CH3COOH (CH3COO)2Mg + H2
(CH3COO)2Mg + H2
CaO + 2CH3COOH (CH3COO)2Ca + H2O
(CH3COO)2Ca + H2O
NaOH + CH3COOH CH3COONa + H2O
CH3COONa + H2O
K2CO3 + 2CH3COOH 2CH3COOK + H2O + CO2
2CH3COOK + H2O + CO2
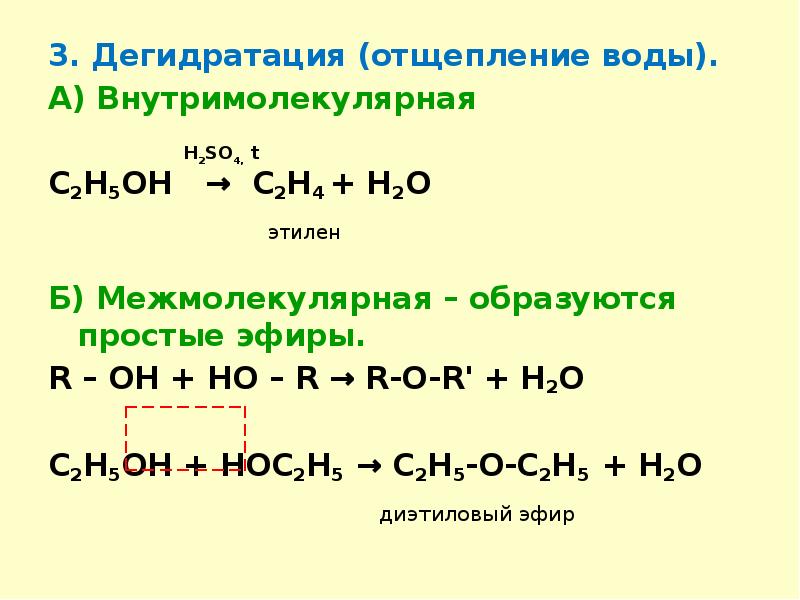
- Этерификация (реакция карбоновых кислот со спиртами, приводящая к образованию сложного эфира):



+ H2O муравьиная кислота этанол этиловый эфир
муравьиной кислоты
В реакцию этерификации могут вступать и многоатомные спирты, например, глицерин. Сложные эфиры, образованные глицерином и высшими карбоновыми кислотами (жирными кислотами) - это жиры.
+ 


+ 3H2O глицерин карбоновые кислоты триглицерид
Жиры представляют собой смеси триглицеридов. Предельные жирные кислоты (пальмитиновая C15H31COOH, стеариновая C17H35COOH) образуют твердые жиры животного происхождения, а непредельные (олеиновая C17H33COOH, линолевая C17H31COOH и др.) - жидкие жиры (масла) растительного происхождения. - Замещение в углеводородном радикале:
CH3—CH2—COOH + Cl2 
CH3—CHCl—COOH + HCl пропионовая кислота  -хлорпропионовая кислота
-хлорпропионовая кислота
Замещение протекает в -положение.
-положение.
Особенность муравьиной кислоты HCOOH состоит в том, что это вещество - двуфункциональное соединение, оно одновременно является и карбоновой кислотой, и альдегидом:
Поэтому муравьиная кислота кроме всего прочего реагирует и с аммиачным раствором оксида серебра (реакция серебряного зеркала; качественная реакция):HCOOH + Ag2O(аммиачный раствор) CO2 + H2O + 2Ag
CO2 + H2O + 2Ag
Получение карбоновых кислот
- Окисление альдегидов.
В промышленности: 2RCHO + O2 2RCOOH
2RCOOH
Лабораторные окислители: Ag2O, Cu(OH)2, KMnO4, K2Cr2O7 и др. - Окисление спиртов: RCH2OH + O2
 RCOOH + H2O
RCOOH + H2O - Окисление углеводородов: 2C4H10 + 5O2
 4CH3COOH + 2H2O
4CH3COOH + 2H2O - Из солей (лабораторный способ): CH3COONaкр. + H2SO4 конц.
 CH
CH
ГРУППА 303 ЭКОЛОГИЯ 15
ТЕМА 15 Дифференцированный зачёт. (ПРОДОЛЖЕНИЕ)
Выполните тест, в конце теста знак "отправить"