ПЯТНИЦА. 20.11.20 г. 206,308, 106, 201,108 ГРУППЫ
ГРУППА 206.
ТЕМА:
|
Межклассовая изомерия с алкадиенами |
Алкадиены
Алкадиены - непредельные (ненасыщенные) углеводороды, имеющие в молекуле две двойных связи С=С. Каждая такая связь содержит одну сигма-связь (σ-связь) и одну пи-связь (π-связь).
Алкадиены также называют диеновыми углеводородами. Первый член гомологического ряда - пропадиен - CH2=C=CH2. Общая формула их гомологического ряда - CnH2n-2.
Номенклатура и изомерия алкадиенов
Названия алкенов формируются путем добавления суффикса "диен" к названию алкана с соответствующим числом: пропадиен, бутадиен, пентадиен и т.д.
При составления названия алкадиена важно учесть, что главная цепь атомов углерода должна обязательно содержать двойные связи. Нумерация атомов углерода в ней начинается с того края, к которому ближе двойная связь. В конце названия указывают атомы углерода, у которых начинается двойная связь.
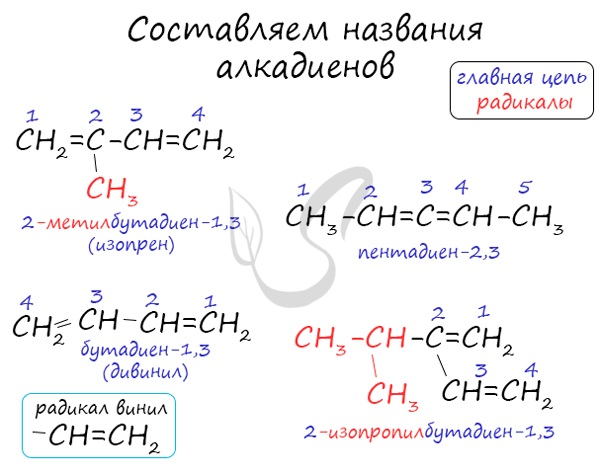
Атомы углерода, прилежащие к двойной связи находятся в sp2 гибридизации.
Для алкадиенов характерна изомерия углеродного скелета, положения двойных связей, межклассовая изомерия с алкинами и пространственная геометрическая изомерия в виде существования цис- и транс-изомеров.
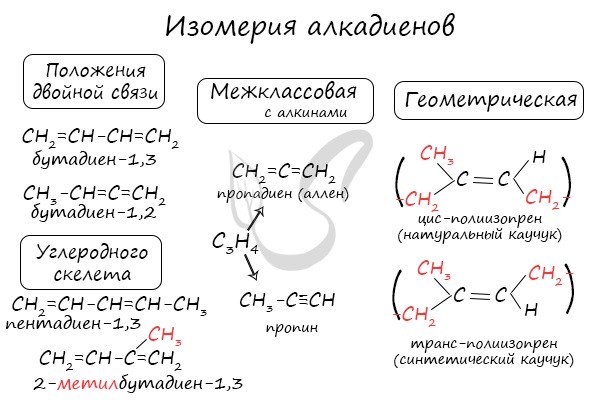
Также к синтетическим каучукам относится бутадиен-1,3 (дивинил).
ПРОВЕРЬТЕ СЕБЯ, ПРОЙДИТЕ ТЕСТ (С ПОДСКАЗКАМИ) ЗДЕСЬ:
https://studarium.ru/article-test/184
ГРУППА 308 Тема:Повторение и обобщение материала темы: «Алканы» .Контрольная работа№1 по теме: «Алканы».
КОНТРОЛЬНАЯ РАБОТА № 1 по
теме: «АЛКАНЫ»
Вариант 1
ЧАСТЬ А
При
выполнении заданий этой части для каждого задания (А1 – А10) запишите
цифру, которая соответствует номеру выбранного вами ответа.
Задание A1
Общая формула циклоалканов
1) СnH2n–6
2) CnH2n–2
3) CnH2n
4) CnH2n+2
Задание A2
Название углеводорода, формула которого C5H12
1) этан
2) пентан
3) бутан
4) пропан
Задание A3
Изомером октана является:
1) 2,3-диметилгептан;
2) 2,3-диметилбутан;
3) 2,3-диметилпентан;
4) 2,3-диметилгексан.
Задание A4
Молекулярная формула
бутана
1) СH4
2) C3H6
3) C4H10
4) C4H8
Задание
A5
Гомологом 2,4-диметилоктана является:
1) 2,5-диметилгептан;
2) 3,3-диметилбутан;
3) 2,3-диметилпентан;
4) 2,4-диметилгексан.
Задание A6
Процесс разложения углеводородов
нефти на более летучие вещества называется
1) крекинг
2) дегидрирование
3) гидрирование
4) дегидратация
Задание A7
Пропан реагируют
1) с водой
2) с раствором KMnO4
3) с водородом
4) с хлором
Задание A8
Сумма коэффициентов в уравнении
реакции полного сгорания этана равна
1) 10
2) 9
3) 19
4) 16
Задание A9
Известно термохимическое
уравнение горения метана CH4
+ 2O2 → CO2
+2H2O + 896 кДж. Какое количество
метана расходуется при выделении 89,6 кДж теплоты?
1) 0,1 моль
2) 0,2 моль
3) 0,25 моль
4) 0,5 моль
Задание A10
Реакция горения алкана
1) 2C3H6
+ 9О2 ®6 CО2 +6 H2О
2) 2С2H2 +5О2 ® 4CО2
+ 2H2О
3) C3H8+
5О2 ® 3CО2
+4 H2О
4) С2H4 +3О2® 2CО2
+ 2H2О
ЧАСТЬ
В
Ответом к заданиям этой части (В1 – В2) является
набор чисел и букв, которые следует записать как соответствия, например: 1-А,
2-Д, 3-Г, 4-В.
Задание B1
Установите
соответствие между формулой органического вещества и названием ,
принадлежащим ему.
ФОРМУЛА
1) СН3 - СН - СН2
- СН2 - СН3
|
СН3
2) СН3 - СН2
- СН2 - СН2 - CH2 - CH3
3) СН3
- СH - CH3 - СН3
|
СН3
4) СН3 - СН - СН - СН2 -
CH2 - CH3
| |
НАЗВАНИЕ ВЕЩЕСТВА НАЗВАНИЕ
ВЕЩЕСТВА
А) 2 - метилбутан
Б) 2 - метилпентан
В) 2 - метил - 3 - этилгексан
Г) гексан
СН3 С2Н5
Задание B2
Установите
соответствие между названием вещества и формулой его гомолога.
НАЗВАНИЕ ВЕЩЕСТВА ФОРМУЛА ГОМОЛОГА
1) циклопентан A) СН3
|
Н3С − С − СН2 − СН3
|
СН3
2) 2,4-диметилгептан Б) CH3
– CH – CH2 – CH – CH3
| |
CH3 CH3
3) Изобутан (2-метилпропан) В) CH2
– CH2
| |
CH2 – CH2
4) 2,2-диметилгексан Г) CH3
– CH2 – CH – CH3
|
CH3
ЧАСТЬ С
При ответе на задания этой части запишите полный ответ
Задание C1
Составьте структурную
формулу органического вещества
2,2,4 –
триметилгексана.
Задание C2
При полном сгорании циклического углеводорода образовался
оксид углерода (IV)
массой
Примерное распределение времени,
отводимое на выполнение отдельных заданий составляет:
для каждого задания части 1–1-2
минуты;
для каждого задания части 2 –
5-7 минут;
для каждого задания части 3 – до
10-12 минут.
Оценки за тестовый вариант контрольной работы:
10 - 13 баллов – оценка «3».
14-17 баллов – оценка «4»
18-21 балл – оценка «5».
ГРУППА 106
ТЕМА:Наследственная изменчивость человека. Лечение и предупреждение некоторых наследственных болезней человека.
Мутационная изменчивость (мутации) — это стойкие внезапно возникшие изменения структуры наследственного материала на различных уровнях его организации, приводящие к изменению тех или иных признаков организма.
Термин «мутация» введен в науку Де Фризом. Им же создана мутационная теория, основные положения которой не утратили своего значения и по сей день.
Основные положения мутационной теории
1. Мутации возникают внезапно, скачкообразно, без всяких переходов.
2. Мутации наследственны, т.е. стойко передаются из поколения в поколение.
3. Мутации не образуют непрерывных рядов, не группируются вокруг среднего типа (как при модификационной изменчивости), они являются качественными изменениями.
4. Мутации ненаправленны — мутировать может любой локус, вызывая изменения как незначительных, так и жизненно важных признаков в любом направлении.
5. Одни и те же мутации могут возникать повторно.
6. Мутации индивидуальны, то есть возникают у отдельных особей.
Процесс возникновения мутаций называют мутагенезом, а факторы среды, вызывающие появление мутаций, — мутагенами.
По типу клеток, в которых мутации произошли, различают: генеративные и соматические мутации.
Генеративные мутации возникают в половых клетках, не влияют на признаки данного организма, проявляются только в следующем поколении.
Соматические мутации возникают в соматических клетках, проявляются у данного организма и не передаются потомству при половом размножении. Сохранить соматические мутации можно только путем бесполого размножения (прежде всего вегетативного).
По адаптивному значению выделяют: полезные, вредные (летальные, полулетальные) и нейтральные мутации. Полезные — повышают жизнеспособность, летальные — вызывают гибель, полулетальные — снижают жизнеспособность, нейтральные — не влияют на жизнеспособность особей. Следует отметить, что одна и та же мутация в одних условиях может быть полезной, а в других — вредной.
По характеру проявления мутации могут быть доминантными и рецессивными. Если доминантная мутация является вредной, то она может вызвать гибель ее обладателя на ранних этапах онтогенеза. Рецессивные мутации не проявляются у гетерозигот, поэтому длительное время сохраняются в популяции в «скрытом» состоянии и образуют резерв наследственной изменчивости. При изменении условий среды обитания носители таких мутаций могут получить преимущество в борьбе за существование.
В зависимости от того, выявлен ли мутаген, вызвавший данную мутацию, или нет, различают индуцированные и спонтанные мутации. Обычно спонтанные мутации возникают естественным путем, индуцированные — вызываются искусственно.
В зависимости от уровня наследственного материала, на котором произошла мутация, выделяют: генные, хромосомные и геномные мутации.
Генные мутации
Генные мутации — изменения структуры генов. Поскольку ген представляет собой участок молекулы ДНК, то генная мутация представляет собой изменения в нуклеотидном составе этого участка. Генные мутации могут происходить в результате:
1) замены одного или нескольких нуклеотидов на другие;
2) вставки нуклеотидов;
3) потери нуклеотидов;
4) удвоения нуклеотидов;
5) изменения порядка чередования нуклеотидов.
Эти мутации приводят к изменению аминокислотного состава полипептидной цепи и, следовательно, к изменению функциональной активности белковой молекулы. Благодаря генным мутациям возникают множественные аллели одного и того же гена.
Заболевания, причиной которых являются генные мутации, называются генными (фенилкетонурия, серповидноклеточная анемия, гемофилия и т.д.). Наследование генных болезней подчиняется законам Менделя.
Хромосомные мутации
Это изменения структуры хромосом. Перестройки могут осуществляться как в пределах одной хромосомы — внутрихромосомные мутации (делеция, инверсия, дупликация, инсерция), так и между хромосомами — межхромосомные мутации
Хромосомные мутации: 1 — парахромосом; 2 — делеция; 3 — дупликация; 4, 5 — инверсия; 6 — инсерция.
Заболевания, причиной которых являются хромосомные мутации, относятся к категории хромосомных болезней. К таким заболеваниям относятся синдром «крика кошки», транслокационный вариант синдрома Дауна и др.
Геномные мутации
Геномной мутацией называется изменение числа хромосом. Геномные мутации возникают в результате нарушения нормального хода митоза или мейоза.
Гаплоидия — уменьшение числа полных гаплоидных наборов хромосом.
Полиплоидия — увеличение числа полных гаплоидных наборов хромосом: триплоиды (3n), тетраплоиды (4n) и т.д.
Гетероплоидия — некратное увеличение или уменьшение числа хромосом. Чаще всего наблюдается уменьшение или увеличение числа хромосом на одну (реже две и более).
Лечение наследственных аномалий обмена веществ. Повышенный интерес медицинской генетики к наследственным заболеваниям объясняется тем, что во многих случаях знание биохимических механизмов развития заболевания позволяет облегчить страдания больного. Больному вводят несинтезирующиеся в организме ферменты или исключают из пищевых рационов продукты, которые не могут быть использованы вследствие отсутствия в организме необходимых для этого ферментов. Заболевание сахарным диабетом характеризуется повышением концентрации сахара в крови вследствие отсутствия инсулина — гормона поджелудочной железы. Это заболевание вызывается рецессивной мутацией. Оно лечится введением в организм инсулина.
Однако следует помнить, что излечивается только болезнь, т. е. фенотипическое проявление вредного гена, и вылеченный человек продолжает оставаться его носителем и может передавать этот ген своим потомкам. Сейчас известны более ста заболеваний, в которых механизмы биохимических нарушений изучены достаточно подробно. В некоторых случаях современные методы микроанализов позволяют обнаружить такие биохимические нарушения даже в отдельных клетках, а это, в свою очередь, позволяет ставить диагноз о наличии подобных заболеваний у еще не родившегося ребенка по отдельным его клеткам, плавающим в околоплодной жидкости беременной женщины.
Нежелательность родственных браков. В современном обществе родственные браки (браки между двоюродными братьями и сестрами) сравнительно редки. Однако есть области, где в силу географических, социальных, экономических или других причин небольшие контингенты населения в течение многих поколений живут изолированно. В таких изолированных популяциях (так называемых изолятах) частота родственных браков по понятным причинам бывает значительно выше, чем в обычных «открытых» популяциях. Статистика свидетельствует, что у родителей, состоящих в родстве, вероятность рождения детей, пораженных теми или иными наследственными недугами, или частота ранней детской смертности в десятки, а иногда даже в сотни раз выше, чем в неродственных браках. Родственные браки особенно нежелательны, когда имеется вероятность гетерозиготности супругов по одному и тому же рецессивному вредному гену.
ГРУППА 201
ТЕМА:
Реакции присоединения (гидрирования, галогенирования, гидрогалогенирования, гидратации).
(дегидрирования, дегидрогалогенирования, дегидратации.)Типы химических реакций в органической химии При протекании химических реакций происходит разрыв одних и возникновение других связей. Химические реакции условно делят на органические и неорганические. Органическими реакциям принято считать реакции, в которых, по крайней мере, одно из реагирующих веществ является органическим соединением, изменяющим свою молекулярную структуру в процессе реакции. Отличием органических реакций от неорганических является то, что, как правило, в них участвуют молекулы. Скорость таких реакции низка, а выход продукта обычно составляет всего лишь 50-80 %. Для повышения скорости реакции применяют катализаторы, повышают температуру или давление. Далее рассмотрим типы химических реакций в органической химии. Классификация по характеру химических превращений
Реакции замещения В ходе реакций замещения один атом или группа атомов в начальной молекуле замещается на иные атомы или группы атомов, образуя новую молекулу. Как правило, такие реакции характерны для насыщенных и ароматических углеводородов, например:
Реакции присоединения При протекании реакций присоединения из двух или более молекул веществ образуется одна молекула нового соединения. Такие реакции характерны для ненасыщенных соединений. Различают реакции гидрирования (восстановления), галогенирования, гидрогалогенирования, гидратации, полимеризации и т.п:
|
|
|







