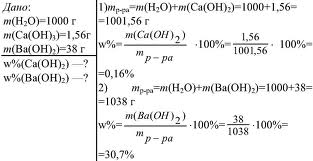ВТОРНИК, 30.11.21 г. 206, 405, 401, 403
ГРУППА 206 БИОЛОГИЯ 53,54
ТЕМА:Развитие жизни в Палеозое.
Палеозойская эра началась около 540 миллионов лет назад и закончилась примерно 250 миллионов лет назад. Она продолжалась 290 миллионов лет. Первый период Палеозойской эры - кембрийский, начался с массового распространения живых организмов с минеральным скелетом. Долгое время считалось, что тогда же возникли и многоклеточные организмы, но изучение вендской (эдиакарской) фауны показало, что мягкотелые многоклеточные, лишенные минерального скелета, возникли значительно раньше. Сейчас палеонтологи полагают, что отдельные виды, обладавшие различными скелетными элементами, могли появится и до начала Палеозоя, но они не были массовыми.
На протяжении Палеозоя возникает огромное количество типов и классов живых существ. Жизнь очень сильно усложняется. Если в самом начале Палеозоя все живые организмы обитают в морях, а самыми развитыми живыми существами являются головоногие моллюски, то в конце последнего периода Палеозойской эры – пермского, на суше, покрытой лесами, уже существуют не только амфибии и рептилии, но и примитивные млекопитающие.
Именно в Палеозое происходит освоение суши, сначала растениями, затем членистоногим, а затем уже и позвоночными. Освоение новой среды обитания приводит к возникновению новых приспособлений и адаптаций, появляются совершенно новые организмы, способные жить в новых условиях. Осваивающие мелководья и полузатопленные участки побережий потомки рыб – амфибии, живут на размытой границе воды и суши, но все-таки еще в воде. Рептилии, благодаря более плотным кожным покровам и размножению защищенными от высыхания, в отличие от икры амфибий, яйцами, уже по-настоящему осваивают сушу.
Морская жизнь не только «выплескивается» на сушу, но и постоянно усложняется в родной среде обитания. Безраздельно властвовавших в начале Палеозоя в толще воды головоногих моллюсков теснят рыбы. Часть головоногих вымирает, но возникают все более сложно организованные виды, появляются аммониты, расцвет которых придется на следующую эру – Мезозойскую.
С середины Палеозоя жизнь начинает осваивать еще одну среду – воздушную. Но пока в воздух поднимаются только членистоногие – насекомые. Для позвоночных воздух еще закрыт – они освоят эту среду только в триасе – первом периоде Мезозоя.
Конечно, на протяжении всего Палеозоя идет не только возникновение новых групп живых организмов, но и вымирание старых, не успевающих приспособится к новой, изменяющейся обстановке. К середине Палеозоя вымирают широко распространенные в кембрии членистоногие хищники – аномалокарисы и подобные им виды. Трилобиты, доминировавшие в донной фауне в начале Палеозоя, и достигавшие в ордовикском периоде длины в 90 сантиметров, в конце Палеозойской эры – в карбоне и перми, становятся редкими и мелкими – 1-2 сантиметра в длину.
А завершается Палеозой грандиозным вымиранием в конце пермского периода. Это вымирание по своим масштабам превзошло все другие известные вымирания, в том числе и знаменитое вымирание динозавров в конце Мезозоя. В конце перми исчезло до 95% видов земной фауны. Причины этого катастрофического вымирания, впрочем, как и других подобных событий, точно неизвестны. Глобальность и массовость вымирания свидетельствуют о том, что у него была какая-то общая и масштабная причина. Сторонники катастроф винят в пермском кризисе мощнейшее извержение вулканов на территории современной Сибири или падение крупного астероида, след от которого пока не найден. Есть предположение, что падение астероида и последовавшая за ним вспышка вулканизма связаны друг с другом. Другие исследователи винят в катастрофе резкое глобальное потепление, перегрев Земли, который привел к уменьшению содержания кислорода в воде океанов и гибели как наземных, так и водных экосистем. Есть и другие гипотезы. Ни одна из них не может сейчас считаться более-менее подтвержденной. Ясно одно – жизнь пережила этот кризис и вышла на новый виток своего развития.
ТЕМА: РАЗВИТИЕ ЖИЗНИ В МЕЗОЗОЕ.


|
|
ГРУППА 405 ХИМИЯ 1,2
ТЕМА: Научные методы познания веществ и химических явлений. Роль эксперимента и теории в химии. Моделирование химических процессов.
ТЕМА: Основные понятия химии. Вещество. Атом. Молекула. Химический элемент. Аллотропия. Простые и сложные вещества. Качественный и количественный состав веществ.
Прежде чем приступить к любой работе и получить определённый результат, человек выбирает наиболее эффективные и доступные способы и приёмы выполнения её, инструмент и приспособления, которые можно использовать для этого, операции, которые необходимо совершить.
Совокупность приёмов и операций практического и теоретического освоения действительности и определяет понятие «метод».
Рассмотрим научные методы познания химии, т.е. методы познания, которые используются для изучения веществ и химических явлений.
Различают 2 уровня научного познания: эмпирический и теоретический.
Методы эмпирического уровня познания
Эмпирический уровень - характеризуется исследованием реально существующих объектов. На этом уровне происходит процесс накопления информации об этих объектах с помощью следующих методов: наблюдение, измерение, постановка экспериментов.
В это же время осуществляется первичная систематизация получаемых фактических данных в виде описания, таблиц, схем, графиков и т.д.
Познакомимся с каждым из этих методов отдельно.
Наблюдение – это первоначальный метод эмпирического познания, позволяющий получить первичную информацию об объекте изучения.
Наблюдение является целенаправленным, планомерным, активным методом научного познания: оно ведётся для решения заранее поставленных задач, строго по составленному исследователем плану, согласованному с поставленными задачами и сопровождается активными действиями исследователя. Результаты научных наблюдений фиксируются в виде описания признаков наблюдаемого объекта, таблиц, схем и т.д. Всё это является базисом науки, опираясь на который учёные создают эмпирические обобщения, сравнивают изучаемые объекты по тем или иным признакам, проводят классификацию, выявляют закономерности.
Наблюдения могут быть непосредственными, воспринимаемыми органами чувств человека, и опосредованными, которые проводятся с использованием технических средств наблюдения: микроскопов, телескопов и др.
В процессе наблюдения могут совершаться открытия новых явлений, позволяющих обосновать какую-либо научную гипотезу или подтвердить какое-либо положение известной теории.
Из всего сказанного следует, что наблюдение является важнейшим методом научного познания, позволяющим собрать обширную информацию об окружающем мире.
Эксперимент – более сложный метод эмпирического познания по сравнению с наблюдением. Он отличается от метода наблюдения тем, что в ходе эксперимента исследователь может изменять условия (давление, температуру, напряжение и т.д.), устранять побочные факторы, затрудняющие процесс исследования. Эксперимент может повторяться несколько раз для получения наиболее достоверных результатов.
Условия научного эксперимента: целенаправленность, наличие базы в виде исходных теоретических положений, наличие плана проведения эксперимента, наличие технических средств, наличие специалистов необходимого уровня квалификации.
В зависимости от характера поставленных задач, решаемых в ходе эксперимента, последние подразделяются на исследовательские и проверочные.
Исследовательские эксперименты направлены на обнаружение новых, неизвестных науке свойств изучаемого объекта. Результатом такого эксперимента могут быть выводы, изменяющие представления об этом объекте.
Проверочные эксперименты служат для проверки или подтверждения тех или иных теоретических положений.
Следующий эмпирический метод познания – измерение.
Измерение – это процесс определения количественных значений свойств изучаемого объекта с помощью специальных технических устройств.
Измерения бывают прямые и косвенные.
Прямые измерения – это такие измерения, при которых значение измеряемой величины выдаётся непосредственно измерительным прибором.
При косвенном измерении искомое значение величины определяют по известной математической зависимости (по формуле), используя для этого данные, полученные при прямых измерениях.
В процессе измерения не всегда требуется участие человека. Измерение может быть включено в работу автоматической информационно-измерительной системы, которая строится на базе электронно-вычислительной техники.
Методы теоретического уровня познания
Идеализация – представляет собой мысленное внесение определенных изменений в изучаемый объект в соответствии с целями исследований. В результате таких изменений могут быть исключены из рассмотрения какие-то свойства, признаки, стороны объектов. Например, в механике идеализация материальной точки как тела, лишенного размеров и массы. Такой прием удобен при описании движения, в том числе атомов и молекул.
Идеализация используется тогда, когда реальные объекты достаточно сложны для имеющихся средств математического анализа, когда некоторые свойства затемняют существо протекающих в объекте процессов.
Роль идеализации как метода научного познания заключается в том, что получаемые на его основе теоретические положения, можно использовать для исследования реальных объектов или явлений.
Формализация - заключается в использовании специальной символики, позволяет отвлечься от изучения реальных объектов и оперировать вместо этого символами (знаками). Достоинством формализации является возможность проведения исследований без обращения к какому-либо объекту, кроме этого обеспечивается краткость и четкость записи научной информации.
Методы, применяемые на эмпирическом и теоретическом уровнях познания
Анализ и синтез.
Под анализом понимают разделение объекта (мысленно или реально) на составные части с целью изучения их по отдельности.
Под синтезом понимают соединение составных частей объекта (мысленно или реально) с целью изучения его как единого целого. Для изучения объекта как единого целого необходимо рассматривать его составные части в совокупности, в единстве. В процессе синтеза производится соединение воедино составных частей изучаемого объекта. Анализ и синтез успешно используются в сфере мыслительной деятельности человека, т.е. в теоретическом познании.
Моделирование – основано на изучении моделированного объекта. Модель строится по подобию оригинала, на ней воспроизводят, свойственные оригиналу процессы и полученные сведения переносятся на моделируемый объект – оригинал.
Различают несколько видов моделирования:
Мысленное. К нему относятся самые различные мыслительные представления в форме тех или иных воображаемых моделей.
Физическое. Оно характеризуется физическим подобием между моделью и оригиналом.
Символическое – связано с построением графиков, схем.
Численное моделирование на ЭВМ.
Моделирование как метод познания бывает единственно необходимым для исследования некоторых явлений.
Таким образом, все названные методы научного познания являются важными и необходимыми для познания окружающего мира.
ТЕМА 2: Основные понятия химии. Вещество. Атом. Молекула. Химический элемент. Аллотропия. Простые и сложные вещества. Качественный и количественный состав веществ.
1.Вещество. Атом. Молекула. Химический элемент. Аллотропия.
Химия– это наука о веществах и процессах их превращения, при которых происходит изменение состава и структуры.
Вещество - это каждый отдельный вид материи, обладающий при данных условиях определенными физическими свойствами (вода, железо, сера, известь, кислород). Природные вещества представляют собой смеси, состоящие иногда из большого числа различных веществ.
Основой всей химической науки являются атомно-молекулярное учение, закон сохранения материи, периодический закон Д.И.Менделеева и теория химического строения.
Создание атомно-молекулярного учения относится к концу 18 - началу 19 вв., когда в химию были введены количественные методы исследования.
Огромный вклад в создание этой теории внес русский ученый М.В.Ломоносов.
Основные положения заключаются в следующем:
1. Вещества состоят из молекул; молекулы различных веществ отличаются между собой химическим составом, размерами, физическими и химическими свойствами.
2. Молекулы находятся в непрерывном движении; между ними существует взаимное притяжение и отталкивание. Скорость движения молекул зависит от агрегатного состояния веществ.
3. При физических явлениях состав молекул остается неизменным, при химических - претерпевают качественные и количественные изменения и из одних молекул образуются другие.
4. Молекулы состоят из атомов. Атомы характеризуются определенными размерами и массой. Свойства атомов одного и того же элемента одинаковы и отличаются от свойств атомов других элементов.
При химических реакциях атомы не претерпевают качественных изменений.
Атом – это электронейтральная частица, состоящего из положительно заряженного ядра и отрицательно заряженных электронов. Атом – наименьшая частичка химического элемента, предел химической делимости материи. Атом- носитель свойств химического элемента.
Атомы могут взаимодействовать между собой, образуя молекулы.
Валентность – это способность атомов элементов образовывать химические связи. Молекула – это система, состоящая из связанных между собой атомов.
Молекула – это наименьшая частица вещества, обладающая его химическими свойствами.
Молекула способная к самостоятельному существованию и состоит из одинаковых или различных атомов, соединенных в одно целое химическими связями.
Химический элемент – это совокупность атомов с одинаковым положительным зарядом ядра.
Каждый химический элемент обозначают соответствующим символом. Символ Cu обозначает атом меди, H- один атом водорода.
Состав веществ обозначают химическими формулами, в которых символами указывают химические элементы, входящие в состав вещества, цифровыми индексами справа – число атомов каждого элемента. В состав молекулы серной кислоты H2SO4 входят два атома водорода, один атом серы и четыре атома кислорода.
Каждая химическая связь в формуле обозначается черточкой.
Способность химического элемента образовывать несколько простых веществ называется аллотропией.
А различные простые вещества, образованные одним элементом, - аллотропными видоизменениями, или аллотропными модификациями.
Явление аллотропии обусловлено несколькими причинами:
- Образованием молекул с различным числом атомов (кислород О2 и озон О3 фосфор двухатомный Р 2 и четырехатомный Р4)
- образованием кристаллов различных модификаций (углерод в виде графита и алмаза).
2.Простые и сложные вещества. Качественный и количественный состав веществ.
Простые вещества – это вещества, образованные одним химическим элементом.
Один и тот же химический элемент может образовывать несколько простых веществ.
Вещества, образованные из двух и более химических элементов, называют сложными. Сложных веществ гораздо больше, чем простых.
Различают в качественный и количественный состав веществ.
Качественный состав – это совокупность химических элементов и (или) атомных группировок, составляющих данное химическое вещество.
Количественный состав – это показатели, характеризующие количество или число атомов того или иного химического элемента и (или) атомных группировок, образующих данное химическое вещество.
Состав веществ отображают посредством химической символики.
По предложению Й. Я. Берцелиуса элементы принято обозначать первой или первой и одной из последующих букв латинских названий элементов.
Контрольные вопросы:
1.Какая связь между понятием «атом» и «молекула»? В чем различие между ними?
2.Чем отличается простое вещество от химического элемента?
ГРУППА 401 ХИМИЯ 19
ТЕМА: Агрегатные состояния веществ и водородная связь. Твердое, жидкое и газообразное состояния веществ. Переход вещества из одного агрегатного состояния в другое. Водородная связь.
ГРУППА 403 ХИМИЯ 28, 29
ТЕМА: Массовая доля растворенного вещества.
Массовая доля.
Один из самых распространенных способов выражения концентрации раствора – через массовую долю растворенного вещества.
Отношение массы растворенного вещества к общей массе раствора называют массовой долей растворенного вещества.
Массовую долю обозначают греческой буквой «омега» и выражают в долях единицы или процентах (рисунок 2).
Рис.2. Массовая доля компонентов смеси.
Посмотрев видео
вы вникнете в понятие массовой доли и научитесь ее вычислять.
Если в 100 г раствора содержится 30 г хлорида натрия, это означает, что ω(NaCl) = 0,3 или ω(NaCl) = 30 %. Можно также сказать: «имеется тридцатипроцентный раствор хлорида натрия».
Массовая доля — самая распространенная в быту и большинстве отраслей промышленности концентрация. Именно массовая доля жира, например, указана на пакетах с молоком (посмотрите на рисунок 3).
Рис.3. Массовая доля жира в молоке.
Масса раствора складывается из массы растворителя и массы растворенного вещества, т. е.:
m(раствора) = m(растворителя) + m(растворенного вещества).
Предположим, массовая доля растворенного вещества равна 0,1, или 10%. Следовательно, оставшиеся 0,9, или 90%, – это массовая доля растворителя.
Массовая доля растворенного вещества широко используется не только в химии, но и в медицине, биологии, физике, да и в повседневной жизни. Рассмотрим решение некоторых задач
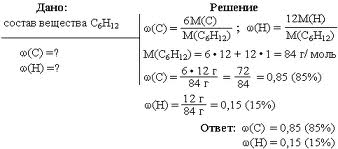
Рис.4. Задача на нахождение массовой доли.
ТЕМА:Электролитическая диссоциация. Электролиты и неэлектролиты.
СМОТРИМ, СЛУШАЕМ, КОНСПЕКТИРУЕМ.