16.04.21 г. 303, 201, 208
ГРУППА 303
ТЕМА 1 :Применение алканов на основе свойств.
Применение
Алканы широко применяются в промышленной химии, косметологии, строительстве. Из соединений изготавливают:
- топливо (бензин, керосин);
- асфальт;
- смазочные масла;
- вазелин;
- парафин;
- мыло;
- лаки;
- краски;
- эмали;
- спирты;
- синтетические ткани;
- каучук;
- адьдегиды;
- пластмассы;
- моющие средства;
- кислоты;
- пропелленты;
- косметические средства.
Алкены. Этилен, его получение (дегидрированием этана, деполимеризацией полиэтилена). Гомологический ряд, изомерия, номенклатура алкенов.
Непредельные углеводороды
К непредельным относят углеводороды, содержащие в молекулах кратные связи между атомами углерода. Непредельными являются алкены, алкины, алкадиены (полиены). Непредельным характером обладают также циклические углеводороды, содержащие двойную связь в цикле (циклоалкены), а также циклоалканы с небольшим числом атомов углерода в цикле (три или четыре атома). Свойство «непредельности» связано со способностью этих веществ вступать в реакции присоединения, прежде всего водорода, с образованием предельных, или насыщенных углеводородов — алканов.
Алкены
Алкены - непредельные (ненасыщенные) ациклические алифатические углеводороды, имеющие в молекуле одну двойную связь С=С. Такая связь содержит одну сигма-связь (σ-связь) и одну пи-связь (π-связь). Своё второе название — олефины — алкены получили по аналогии с жирными непредельными кислотами (олеиновая, линолевая), остатки которых входят в состав жидких жиров — масел.
Алкены также называют этиленовыми углеводородами, по первому члену гомологического ряда - этилену - CH2=CH2. Общая формула их гомологического ряда - CnH2n.
Гомологический ряд алкенов | Структурные формулы | Названия, суффикс ен, илен |
C2Н4 | CH2=CH2 | этен, этилен |
C3H6 | CH2=CH-CH3 | пропен |
C4H8 | CH2=CH-CH2-CH3 | бутен-1 |
CH3-CH=CH-CH3 | бутен-2 |
Гомологи
СH2=CH2 этен
СH2=CH-CH3 пропен
СH2=CH-CH2-CH3 бутен-1
СH2=CH-CH2-CH2-СН3 пентен-1
Физические свойства алкенов
Этилен (этен) – бесцветный газ с очень слабым сладковатым запахом, немного легче воздуха, малорастворим в воде.
С2 – С4 (газы)
С5 – С17 (жидкости)
С18 – (твёрдые)
§ Алкены не растворяются в воде, растворимы в органических растворителях (бензин, бензол и др.)
§ Легче воды
§ С увеличением Mr температуры плавления и кипения увеличиваются
Строение
Этилен – простейший представитель
Молекулярная формула – С2Н4
Электронная формула | |
Структурная формула | |
Пространственное строение | В молекуле этилена подвергаются гибридизации одна s- и две p-орбитали атомов C – sp2-гибридизация: Таким образом, каждый атом C имеет по три гибридных орбитали (идут на образование трёх σ-связей) и по одной негибридной p-орбитали (идут на образование одной p-связи): |
Запомните характеристики sр2 –гибридизации
1) Плоское тригональное (треугольное) строение
2) Угол – HCH - 120°
3) Длина (-С=С-) связи – 0,134 нм
4) Связи - σ, p
5) Невозможно вращение относительно (-С=С-) связи
Изомерия
Структурная изомерия алкенов
1. Изомерия углеродного скелета (начиная с С4Н8):
2. Изомерия положения двойной связи (начиная с С4Н8):
3. Межклассовая изомерия с циклоалканами, начиная с С3Н6:
Пространственная изомерия алкенов
Вследствие жесткой закрепленности атомов С возможна цис-транс-изомерия.
Номенклатура
Названия алкенов формируются путем добавления суффикса "ен" к названию алкана с соответствующим числом: этен, пропен, бутен, пентен и т.д.
При составлении названия алкена важно учесть, что главная цепь атомов углерода должна обязательно содержать двойную связь. Принято начинать нумерацию атомов углерода с того края, к которому ближе двойная связь. В конце названия указывают атом углерода, у которого начинается двойная связь.
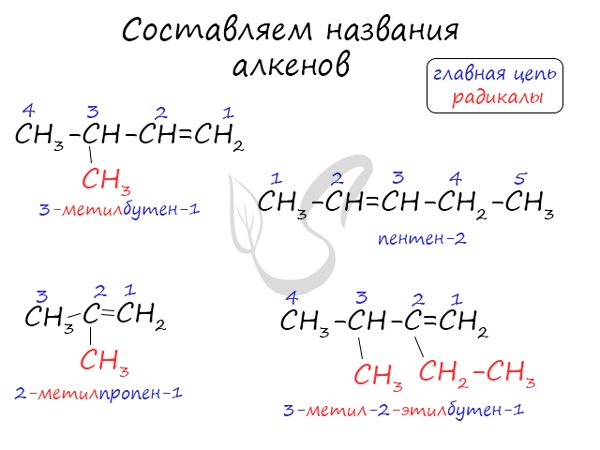
Образование названий алкенов по номенклатуре ИЮПАК
Практическая работа №6
Цель работы: научиться различать органические и неорганические вещества.
(повторите правила ТБ :
Правила техники безопасности при работе в химическом кабинете.
Не трогайте вещества, посуду и не приступайте к работе без разрешения учителя.
Запрещается! Запрещается брать вещества руками и пробовать на вкус.
При выяснении запаха веществ нельзя подносить сосуд близко к лицу, так как вдыхание паров и газов может вызвать раздражение дыхательных путей. Для ознакомления с запахом нужно ладонью руки сделать движение от отверстия сосуда к носу.
Не наливайте и не перемешивайте реактивы вблизи лица. При нагревании нужно направлять отверстие пробирки или колбы в сторону от себя и соседей.
Без указания учителя не смешивайте неизвестные вам вещества.
При выполнении опытов пользуйтесь небольшими дозами веществ. Вещества берите только шпателем или ложечкой и в тех количествах, которые указаны в описании работы; если таких указаний нет, то объемы веществ не должны превышать 1 смᶟ.
Особую осторожность соблюдайте при работе с кислотами и щелочами. Если случайно кислота попадет на руки или одежду, то немедленно смойте ее большим количеством воды.
При разбавлении кислот водой всегда помните следующее правило: кислоты следует медленно тонкой струйкой при перемешивании наливать в воду, а не наоборот.
Всегда пользуйтесь только чистой лабораторной посудой.
Остатки вещества не высыпайте и не выливайте обратно в сосуд с чистыми веществами.
Горячую посуду по внешнему виду невозможно отличить от холодной. Прежде, чем взять посуду рукой, убедитесь, что она остыла. В случае термического ожога нужно охладить обожженную поверхность (холодной водой, льдом из холодильника) и обработать противоожоговой мазью или аэрозолем; если ожог сильный – обратитесь к врачу.
Не бросайте в раковину фильтровальную бумагу, вату, стекла от разбитой посуды.
Перед работой с опасными химическими реактивами (щелочами, кислотами и др.) составьте план эксперимента, наденьте защитный щиток или очки.
При работе со спиртовкой и электронагревательными приборами соблюдайте следующие правила:
Пользуясь спиртовкой, нельзя ее зажигать то другой спиртовки, ибо может пролиться спирт и возникнет пожар.
Чтобы погасить пламя спиртовки, ее следует закрыть колпачком.
Перед включением электронагревателя в сеть проверьте, не повреждена ли изоляция электрического провода нагревателя.
Если при включении электронагревателя в сеть не происходит нагревание, сообщите об этом учителю.
При работе с электронагревателем не допускайте загрязнения спирали накаливания.
После окончания работы обязательно отключите электронагреватель от сети.)
Ход работы:
Задание 1
С помощью качественных реакций определите, в какой из выданных вам пробирок находятся растворы: хлорида натрия, карбоната натрия, сульфата натрия, ацетата натрия.
Задание 2
С помощью качественных реакций определите, в какой из выданных вам пробирок находятся растворы: хлорида аммония, хлорида бария, хлорида алюминия.
Задание 3
С помощью одного реактива определите, в какой из выданных вам пробирок находятся растворы: глюкозы, глицерина, белка.
Задание 4
С помощью индикаторной бумажки определите, в какой из выданных вам пробирок находятся растворы солей: ацетата натрия, нитрат аммония, сульфат калия.
Ацетат натрия: лакмусовая бумажка синяя.
Нитрат аммония: лакмусовая бумажка красная.
Сульфат калия: лакмусовая бумажка не окрашивается.










Комментариев нет:
Отправить комментарий