Здравствуйте, уважаемые студенты, записывайте дату, тему и выполняйте необходимые записи(ВСЁ подряд не пишите, читайте, выбирайте, можно составить план, ЕСЛИ ЕСТЬ ВИДЕО, НАДО ПОСМОТРЕТЬ ,ВЫПОЛНИТЬ ПО НЕМУ ЗАПИСИ, МНОГО НЕ НУЖНО ПИСАТЬ. Материала может быть выложено много, но это не значит, что всё надо записывать! После этого, сфотографируйте и отошлите мне на почту rimma.lu@gmail.com Тетрадь привезете, когда перейдем на очную форму обучения.)
Моя почта : rimma.lu@gmail.com Жду ваши фотоотчеты!
СПРАВА НАХОДИТСЯ АРХИВ- ТАМ СМОТРИМ ДАТУ И ГРУППЫ
РАСПИСАНИЕ ЗАНЯТИЙ НА НЕДЕЛЮ: 03.04.23г. - 07.04.23г.
Пн. 03.04: 506,403
Вт. 04.04::508, 505, 505, 501
Ср. 05.04: 505
Чт. 06.04: 505, 508
Пт. 07.04: 505
ГРУППА 506 ХИМИЯ 21,22
ТЕМА: Состав смесей: объемная и массовая доли компонентов смеси, массовая доля примесей.
Дисперсные системы. Понятие о дисперсной системе. Дисперсная фаза и дисперсионная среда. Классификация дисперсных систем. Понятие о коллоидных системах.
ГРУППА 403 ХИМИЯ 20, 21
ТЕМА:Анилин, как органическое основание. Получение анилина из нитробензола. Применение анилина на основе свойств. Аминокислоты.Белки. Первичная, вторичная, третичная структуры белков
Амины – класс органических соединений, производные аммиака (NH3
СТРОЕНИЕ И КЛАССИФИКАЦИЯ АМИНОВ
Поскольку амины являются продуктами замещения водорода в аммиаке, то все они являются донорами электронной пары, принадлежащей атому азота, то есть проявляют свойства оснований (по Льюису).

Амины классифицируют:
1. По степени замещенности атомов водорода в молекуле аммиака на
- первичные амины ;
- вторичные
- третичные
- четвертичные соли аминов

Радикалы, входящие в молекулу амина могут быть одинаковыми или разными.
2. По типу радикала выделяют амины алифатического и ароматического ряда. Типичным представителем ряда ароматических аминов является анилин

Изомерия алифатических аминов
Для алифатических аминов характерна следующая изомерия:
- углеродного скелета (степени разветвленности углеводородного радикала) начиная с

- положение аминогруппы, начиная с

- изомерия аминогруппы (межклассовая изомерия), связанная с изменением степени замещенности атомов водорода при азоте. Поэтому первичные, вторичные и третичные амины изомерны друг другу:

- пространственная изомерия (оптическая, начиная с бутиламина)

НОМЕНКЛАТУРА АМИНОВ
1. По систематической номенклатуре амины называют путем добавления суффикса "амин" к названию углеводорода.
2. По рациональной номенклатуре их рассматривают как алкил- или ариламины.

У ароматических аминов в основе названия также лежит слово амин, кроме того такие соединения имеют тривиальные названия:

3. Первичные амины часто называют как производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на аминогруппы -
ФИЗИЧЕСКИЕ СВОЙСТВА
Первые представители ряда аминов - метиламин, диметиламин и триметиламин – газы. Остальные низшие амины – жидкости. Обладают резким характерным удушливым запахом. Канцерогены. Высшие амины – твердые вещества, без запаха. Первые представители аминов хорошо растворимы в воде. Высшие амины в воде не растворяются. Это связано с тем, что связь N–H более полярна, чем связь С–H, но менее полярна, чем связь C–O, поэтому водородные связи между молекулами аминов выражены слабее, чем, например, в молекулах спиртов.
Основные представителя ряда аминов
Алкиламины
Метиламин
По своим химическим свойствам метиламин является типичным первичным амином, то есть подобно аммиаку, образует четвертичные соли с кислотами и реагирует с водой, образуя донорно-акцепторную связь, при взаимодействии со сложными эфирами или ацилхлоридами дает амиды (подробнее см. тему: "Производные карбоновых кислот. Амиды. Ангидриды. Хлорангидриды")
Триметиламин
ТЕМА 43: Анилин, как органическое основание. Получение анилина из нитробензола. Применение анилина на основе свойств. Ароматические аминыАнилин
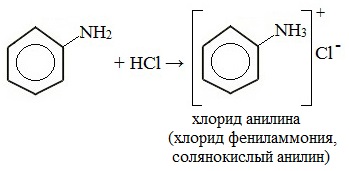
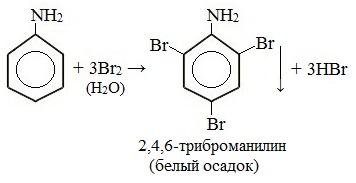
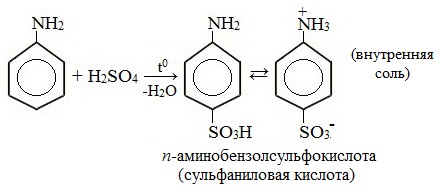
Токсическое действие анилинаАнилин ядовит, действует на центральную нервную систему, вызывает в крови образование метгемоглобина и дегенеративные изменения эритроцитов, гемолиз, следствием чего является кислородное голодание организма. Анилин проникает в организм через органы дыхания в виде паров, а также при всасывании через кожу и слизистые оболочки, которое особенно усиливается при повышении температуры воздуха и приёме алкоголя. Возможны острые и хронические (анилизм) отравления анилином. При лёгком отравлении анилином наблюдаются слабость, головокружение, головная боль, синюшность губ, ушных раковин, ногтей. При отравлениях средней тяжести присоединяется тошнота, иногда рвота, появляется шатающаяся походка; пульс учащён. Тяжёлые случаи отравления встречаются крайне редко. При хронических отравлениях — токсический гепатит, нервно-психические нарушения, расстройство сна, снижение памяти и т. д. Для анилина характерны реакции как по аминогруппе, так и по бензольному кольцу. Особенности этих реакций обусловлены взаимным влиянием атомов. С одной стороны, бензольное кольцо ослабляет основные свойства аминогруппы по сравнению алифатическими аминами и даже с аммиаком. С другой стороны, под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения, чем бензол. I. Основные свойстваУменьшение электронной плотности на атоме азота приводит к снижению способности отщеплять протоны от слабых кислот. Анилин более слабое основание, чем предельные амины и аммиак. Поэтому анилин взаимодействует лишь с сильными кислотами (HCl, H2SO4) и, в отличие от алифатических аминов и аммиака, не образует с водой гидроксида, а его водный раствор не окрашивает лакмус в синий цвет. Анилин с водой не реагирует и не изменяет окраску индикатора!!! Видеоопыт «Изучение среды раствора анилина» Соли анилина, в отличие от анилина, хорошо растворимы в воде. II. Особые свойства анилинаРеакции с участием аминогруппы 1. Взаимодействие с кислотами (образование солей) Анилин реагирует с сильными кислотами, образуя соли фениламмония, которые растворимы в воде, но не растворимы в неполярных органических растворителях: Видеоопыт «Взаимодействие анилина с соляной кислотой» Анилин, который практически не растворяется в воде, можно растворить в соляной кислоте и отделить нерастворимые примеси. Солянокислый анилин хорошо растворим в воде. Если к такому раствору добавить достаточное количество щелочи, то анилин снова выделится в свободном виде: Реакции с участием бензольного ядра Аминогруппа как заместитель I рода облегчает реакции замещения в бензольном ядре, при этом заместители становятся в орто- и пара-положения к аминогруппе. При бромировании анилин легко образует 2, 4, 6 — тризамещенные продукты реакции. По той же причине анилин легко окисляется. 1. Галогенирование Анилин энергично реагирует с бромной водой с образованием белого осадка 2,4,6-триброманилина. Эта реакция может использоваться для качественного и количественного определения анилина: Качественная реакция на анилин! Видеоопыт «Бромирование анилина» Сульфаниловая кислота является важным промежуточным продуктом в синтезе лекарственных веществ (сульфаниламидных препаратов). III. Окисление анилинаАнилин легко окисляется различными окислителями с образованием ряда соединений, поэтому он темнеет при хранении. При действии хлорной извести Ca (Cl) OCl на водный раствор анилина появляется интенсивное фиолетовое окрашивание. Качественная реакция на анилин! Видеоопыт «Окисление анилина раствором хлорной извести – качественная реакция» При взаимодействии анилина с хромовой известью (смесь концентрированной серной кислоты и дихромата калия К2Cr2O7) образуется черный осадок, называемый черным анилином (краситель «анилиновый черный»). Черный анилин применяется как прочный краситель (для окраски тканей и меха в черный цвет). Обычно ткань сначала пропитывают раствором окислителя. Образующийся черный анилин откладывается в порах волокна. Он не растворим в воде и устойчив к мылу и свету. Видеоопыт «Окисление анилина раствором дихроматом калия – получение красителей» IV. Диазотирование анилинаПрактическое значение имеет реакция взаимодействия анилина с азотистой кислотой при пониженной температуре (около 0°С). В результате этой реакции (реакции диазотирования) образуются соли диазония, которые используются в синтезе азокрасителей и ряда других соединений. При более высокой температуре реакция идет с выделением азота и анилин превращается в фенол: Подобно анилину реагируют с азотистой кислотой и другие первичные ароматические амины. Анилин широко применяется в производстве синтетических красителей. Он также входит в состав типографских красок и красителей для тканей. Используется в производстве лекарственных средств (сульфаниламидные препараты), смол, лаков, духов, кремов для обуви, фотографических химикалий, взрывчатых веществ, гербицидов и фунгицидов. Анилин находит применение в качестве вулканизатора каучука, антиоксиданта и антиозонового средства. Белки (протеины, полипептиды) — самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. В состав молекул белков входят атомы углерода, кислорода, водорода, азота и иногда серы, фосфора и железа. Мономерами белков являются аминокислоты, которые (имея в своём составе карбоксильную и аминогруппы) обладают свойствами кислоты и основания (амфотерны).  Благодаря этому аминокислоты могут соединяться друг с другом (их количество в одной молекуле может достигать нескольких сотен). В связи с этим молекулы белков имеют большие размеры, и их называют макромолекулами.  Структура белковой молекулы Под структурой белковой молекулы понимают её аминокислотный состав, последовательность мономеров и степень скрученности молекулы белка. В молекулах белков встречается всего
 Структура белков может нарушаться (подвергаться денатурации) при нагревании, обработке некоторыми химическими веществами, облучении и др. При слабом воздействии распадается только четвертичная структура, при более сильном — третичная, а затем — вторичная, и белок остаётся в виде полипептидной цепи. В результате денатурации белок теряет способность выполнять свою функцию. Нарушение четвертичной, третичной и вторичной структур обратимо. Этот процесс называют ренатурацией.  Разрушение первичной структуры необратимо. Кроме простых белков, состоящих только из аминокислот, есть ещё и сложные белки, в состав которых могут входить углеводы (гликопротеины), жиры (липопротеины), нуклеиновые кислоты (нуклеопротеины) и др. |


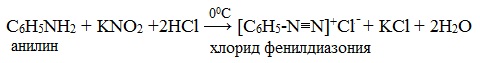
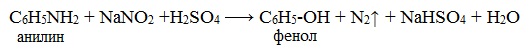
Комментариев нет:
Отправить комментарий