Здравствуйте, уважаемые студенты, записывайте дату, тему и выполняйте необходимые записи(ВСЁ подряд не пишите, читайте, выбирайте, можно составить план, ЕСЛИ ЕСТЬ ВИДЕО, НАДО ПОСМОТРЕТЬ ,ВЫПОЛНИТЬ ПО НЕМУ ЗАПИСИ, МНОГО НЕ НУЖНО ПИСАТЬ. Материала может быть выложено много, но это не значит, что всё надо записывать! После этого, сфотографируйте и отошлите мне на почту rimma.lu@gmail.com Тетрадь привезете, когда перейдем на очную форму обучения.)
Моя почта : rimma.lu@gmail.com Жду ваши фотоотчеты!
СПРАВА НАХОДИТСЯ АРХИВ- ТАМ СМОТРИМ ДАТУ И ГРУППЫ
ГРУППА 506 ХИМИЯ
ТЕМА:Окислительно-восстановительные реакции. Степень окисления. Окислитель и восстановление. Восстановитель и окисление. Метод электронного баланса для составления уравнений окислительно-восстановительных реакций.
Окислительно-восстановительные реакции. Степень окисления. Окислитель и восстановление. Восстановитель и окисление. Метод электронного баланса для составления уравнений окислительно-восстановительных реакций.
Уравнения окислительно-восстановительных реакций.
Многие химические реакции уравниваются простым подбором коэффициентов. Но иногда возникают сложности: количество атомов какого-нибудь элемента в левой и правой частях уравнения никак не удается сделать одинаковым без того, чтобы не нарушить "равновесия" между атомами других элементов.
Чаще всего такие сложности возникают в уравнениях окислительно-восстановительных реакций. Для их уравнивания используют несколько способов, из которых мы пока рассмотрим один – метод электронного баланса.
Напишем уравнение реакции между алюминием и кислородом:
Al + O2 = Al2O3
Пусть вас не вводит в заблуждение простота этого уравнения. Наша задача – разобраться в методе, который в будущем позволит вам уравнивать гораздо более сложные реакции.
Итак, в чем заключается метод электронного баланса? Баланс – это равенство. Поэтому следует сделать одинаковым количество электронов, которые отдает один элемент и принимает другой элемент в данной реакции. Первоначально это количество выглядит разным, что видно из разных степеней окисления алюминия и кислорода:
0 | 0 | +3 –2 | ||
Al | + | O2 | = | Al2O3 |
Алюминий отдает электроны (приобретает положительную степень окисления), а кислород – принимает электроны (приобретает отрицательную степень окисления). Чтобы получить степень окисления +3, атом алюминия должен отдать 3 электрона. Молекула кислорода, чтобы превратиться в кислородные атомы со степенью окисления -2, должна принять 4 электрона:
`
Чтобы количество отданных и принятых электронов выровнялось, первое уравнение надо умножить на 4, а второе – на 3. Для этого достаточно переместить числа отданных и принятых электронов против верхней и нижней строчки так, как показано на схеме вверху.
Если теперь в уравнении перед восстановителем (Al) мы поставим найденный нами коэффициент 4, а перед окислителем (O2) – найденный нами коэффициент 3, то количество отданных и принятых электронов выравнивается и становится равным 12. Электронный баланс достигнут. Видно, что перед продуктом реакции Al2O3 необходим коэффициент 2. Теперь уравнение окислительно-восстановительной реакции уравнено:
4Al + 3O2 = 2Al2O3
Все преимущества метода электронного баланса проявляются в более сложных случаях, чем окисление алюминия кислородом. Например, известная всем "марганцовка" – марганцевокислый калий KMnO4 – является сильным окислителем за счет атома Mn в степени окисления +7. Даже анион хлора Cl– отдает ему электрон, превращаясь в атом хлора. Это иногда используют для получения газообразного хлора в лаборатории:
+7 | –1 | 0 | +2 | |||||||||
KMnO4 | + | KCl | + | H2SO4 | = | Cl2 | + | MnSO4 | + | K2SO4 | + | H2O |
Составим схему электронного баланса:
Двойка и пятерка – главные коэффициенты уравнения, благодаря которым удается легко подобрать все другие коэффициенты. Перед Cl2 следует поставить коэффициент 5 (или 2·5 = 10 перед KСl), а перед KMnO4 – коэффициент 2. Все остальные коэффициенты привязывают к этим двум коэффициентам. Это гораздо легче, чем действовать простым перебором чисел.
2KMnO4 + 10KCl + 8H2SO4 = 5Cl2 + 2MnSO4 + 6K2SO4 + 8H2O
Чтобы уравнять количество атомов К (12 атомов слева), надо перед K2SO4 в правой части уравнения поставить коэффициент 6. Наконец, чтобы уравнять кислород и водород, достаточно перед H2SO4 и H2O поставить коэффициент 8. Мы получили уравнение в окончательном виде.
Метод электронного баланса, как мы видим, не исключает и обыкновенного подбора коэффициентов в уравнениях окислительно-восстановительных реакций, но может заметно облегчить такой подбор.
** Окислительно-восстановительные реакции играют огромную роль в природе и технике. Без этих реакций невозможна жизнь, потому что дыхание, обмен веществ, синтез растениями клетчатки из углекислого газа и воды – все это окислительно-восстановительные процессы.
В технике с помощью реакций этого типа получают такие важные вещества как аммиак (NH3), серную (H2SO4)и соляную (HCl) кислоты и многие другие продукты. Вся металлургия основана на восстановлении металлов из их соединений – руд. Большинство химических реакций – окислительно-восстановительные. Приведем важнейшие определения, связанные с окислительно-восстановительными реакциями.
Реакции, протекающие с изменением степени окисления атомов, входящих в состав реагирующих веществ, называются окислительно-восстановительными.
Окислителями называются вещества, присоединяющие электроны. Во время реакции они восстанавливаются.
Восстановителями называются вещества, отдающие электроны. Во время реакции они окисляются.
Поскольку окислитель присоединяет электроны, степень окисления его атомов может только уменьшаться. Наоборот, восстановитель теряет электроны и степень окисления его атомов должна повышаться.
Окисление всегда сопровождается восстановлением и, наоборот, восстановление всегда связано с окислением.
Число электронов, отдаваемых восстановителем, равно числу электронов, присоединяемых окислителем.
Если каждый атом окислителя может принять иное количество электронов, чем отдает атом восстановителя, то необходимо так подобрать количество атомов того и другого реагента, чтобы количество отдаваемых и принимаемых электронов стало одинаковым. Это требование положено в основу метода электронного баланса, с помощью которого уравнивают уравнения окислительно-восстановительных реакций.
Различают три основных типа окислительно-восстановительных реакций:
1) Реакции МЕЖМОЛЕКУЛЯРНОГО окисления-восстановления (когда окислитель и восстановитель – разные вещества);
2) Реакции ДИСПРОПОРЦИОНИРОВАНИЯ (когда окислителем и восстановителем может служить одно и то же вещество);
3) Реакции ВНУТРИМОЛЕКУЛЯРНОГО окисления-восстановления (когда одна часть молекулы выступает в роли окислителя, а другая – в роли восстановителя).
Рассмотрим примеры реакций трех типов.
1. Реакциями межмолекулярного окисления-восстановления являются все уже рассмотренные нами в этом параграфе реакции.
Рассмотрим несколько более сложный случай, когда не весь окислитель может быть израсходован в реакции, поскольку часть его участвует в обычной – не окислительно-восстановительной реакции обмена:
0 | +5 | +2 | +2 | |||||
Cu | + | HNO3 | = | Cu(NO3)2 | + | NO | + | H2O |
Часть частиц NO3- участвует в реакции в качестве окислителя, давая оксид азота NO, а часть ионов NO3- в неизменном виде переходит в соединение меди Cu(NO3)2. Составим электронный баланс:
Поставим найденный для меди коэффициент 3 перед Cu и Cu(NO3)2. А вот коэффициент 2 следует поставить только перед NO, потому что весь имеющийся в нем азот участвовал в окислительно-восстановительной реакции. Было бы ошибкой поставить коэффициент 2 перед HNO3, потому что это вещество включает в себя и те атомы азота, которые не участвуют в окислении-восстановлении и входят в состав продукта Cu(NO3)2 (частицы NO3- здесь иногда называют “ионом-наблюдателем”).
Остальные коэффициенты подбираются без труда по уже найденным:
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
2. Реакции диспропорционирования происходят тогда, когда молекулы одного и того же вещества способны окислять и восстанавливать друг друга. Это становится возможным, если вещество содержит в своем составе атомы какого-либо элемента в ПРОМЕЖУТОЧНОЙ степени окисления. Следовательно, степень окисления способна как понижаться, так и повышаться. Например:
+3 | +5 | +2 | ||||
HNO2 | = | HNO3 | + | NO | + | H2O |
Эту реакцию можно представить как реакцию между HNO2 и HNO2 как окислителем и восстановителем и применить метод электронного баланса:
+3 | +3 | +5 | +2 | |||||
HNO2 | + | HNO2 | = | HNO3 | + | NO | + | H2O |
Получаем уравнение:
2HNO2 + 1HNO2 = 1HNO3 + 2NO + H2O
Или, складывая вместе моли HNO2:
3HNO2 = HNO3 + 2NO + H2O
3. Реакции внутримолекулярного окисления-восстановления происходят тогда, когда в молекуле соседствуют атомы-окислители и атомы-восстановители. Рассмотрим разложение бертолетовой соли KClO3 при нагревании:
+5 | –1 | 0 | ||
KClO3 | = | KCl | + | O2 |
Это уравнение также подчиняется требованию электронного баланса:
Здесь возникает сложность – какой из двух найденных коэффициентов поставить перед KClO3 – ведь эта молекула содержит и окислитель и восстановитель? В таких случаях найденные коэффициенты ставятся перед продуктами:
KClO3 = 2KCl + 3O2
Теперь ясно, что перед KClO3 надо поставить коэффициент 2.
2KClO3 = 2KCl + 3O2
Внутримолекулярная реакция разложения бертолетовой соли при нагревании используется при получении кислорода в лаборатории.
Мы рассмотрели важнейшие типы окислительно-восстановительных реакций и метод электронного баланса, но пока не касались вопроса составления уравнений таких реакций. Распространенное заблуждение заключается в том, что вы можете сразу предсказать продукт (или продукты) окислительно-восстановительной реакции. Это не так. Лишь по мере накопления опыта, особенно в лаборатории, вы сможете делать все больше и больше правильных предсказаний. А пока следует научиться уравнивать реакции, реагенты и продукты которых заранее известны.
Горение алюминия на воздухе.
Алюминий - активный металл, но из-за очень прочной оксидной пленки на его поверхности не реагирует при обычных условиях с водой и не окисляется. Однако если алюминий перевести в раздробленное состояние - алюминиевую пыль, то он легко сгорает на воздухе. Поместим в пробирку немного алюминиевой пыли и закроем ее пробкой с двумя трубками, одна из которых доходит почти до дна, а другая заканчивается недалеко от пробки. По длинной трубке подадим в пробирку ток воздуха. Струю воздуха, выходящую из короткой трубки и содержащую частички алюминия, направим в пламя горелки. Попадая в пламя, алюминий сгорает яркими вспышками.
4Al + 3O2 = 2Al2O3
Оборудование: штатив, пробирка с боковым отростком, газоотводная трубка, горелка, штапель.
Техника безопасности. Соблюдать правила пожарной безопасности и правила работы с нагревательными приборами. Не направлять пламя в сторону находящихся рядом людей.
ТЕМА: Скорость химических реакций. Понятие о скорости химических реакций. Зависимость скорости химических реакций от различных факторов.
Скорость химической реакции.
«Это
Почти неподвижности мука -
Мчаться куда-то со скоростью звука,
Зная прекрасно, что есть уже где-то
Некто,
Летящий
Со скоростью
Света! »
Леонид Мартынов
Ребята, сегодня на уроке у нас очень интересная и очень важная в изучении химических реакций тема. Но начать урок я хочу с интересных фактов:
- При кипячении воды, ее молекулы движутся со скоростью 650 метров в секунду.
- Ураган может двигаться со скоростью 125 миль в час.
- Ночью волосы растут медленно. Днём рост волос ускоряется. Между 10 и 11 часами скорость роста самая большая. Пик роста наступает между 14 и 16 часами.
- Кровь движется быстро в артериях (500 мм/с), медленнее в венах(150 мм/с), и еще медленнее в капиллярах(1мм/с).
-Самое медлительное млекопитающее в мире — ленивец. Он перемещается со скоростью около двух метров в минуту.
-Самые сильные ветра на Земле дуют в Антарктиде, в долине Виктории. Скорость ветра там достигает 215 метров в секунду.
Ребята, скажите, что объединяет эти научные факты? (в них говорится о скорости).
Следовательно, о чем мы будем говорить сегодня на уроке? (скорости)
Сегодня мы будем говорить о скорости. Но не о той, с которой вы знакомились на уроках физики и математики, а о скорости химических реакций. Итак, тема сегодняшнего урока «Скорость химических реакций»(запишите тему в тетрадь).
Как вы думаете, какие вопросы помогут нам раскрыть тему урока?
(1. Что такое скорость химических реакций? 2. От чего зависит скорость химических реакций?).
ПОСМОТРИТЕ ВНИМАТЕЛЬНО ВИДЕО и ответьте на вопросы.
1. Что такое скорость химических реакций? 2. От чего зависит скорость химических реакций?
На уроке проводятся эксперименты, демонстрирующие зависимость скорости химической реакции от различных факторов. Из материалов данного урока вы узнаете, как влияют на скорость химической реакции степень измельчения, концентрация и природа веществ, а также температура и наличие катализатора.
- Изучение влияния природы кислоты
В одну пробирку наливаем раствор соляной кислоты, а в другую – столько же уксусной (примерно одинаковой концентрации). Одновременно помещаем в них по грануле цинка. В обеих пробирках протекает реакция замещения с выделением водорода:
Zn + 2HCl = ZnCl2 + H2↑
Zn + 2CH3COOH = Zn(CH3CОО)2 + H2↑
В пробирке с уксусной кислотой водород выделяется с меньшей скоростью. Это можно объяснить тем, что уксусная кислота обладает меньшими кислотными свойствами по сравнению с соляной кислотой.
- Изучение влияния природы металла
В две пробирки нальем одинаковое количество соляной кислоты и одновременно поместим в них по кусочку металлов разной природы: цинка и магния. Уравнения данных реакций:
Zn + 2HCl = ZnCl2 + H2↑
Mg + 2HCl = MgCl2 + H2↑
Реакция соляной кислоты с магнием протекает с большей скоростью, так как интенсивнее выделяется водород. Магний – более активный металл, чем цинк (магний стоит в ряду напряжений левее цинка). Рис. 1.

Рис. 1. Результаты опыта по взаимодействия цинка (слева) и магния (справа) с соляной кислотой
ОПЫТ № 2. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ПЛОЩАДИ ПОВЕРХНОСТИ СОПРИКОСНОВЕНИЯ РЕАГИРУЮЩИХ ВЕЩЕСТВ
- Изучение влияния степени измельчения вещества (поверхности соприкосновения реагирующих веществ).
В две пробирки нальем примерно по 2 мл раствора медного купороса. Одновременно поместим в одну пробирку кусок железной проволоки, а в другую – железный порошок. В обеих пробирках протекает реакция замещения в соответствии с уравнением:
Fe + CuSO4 = FeSO4 + Cu↓
О протекании реакции замещения между сульфатом меди (II) и железом можно судить по выделению из раствора вещества красно-бурого цвета – меди. Признаки реакции быстрее появились в пробирке с порошком железа, т. к. порошок железа имеет большую площадь поверхности соприкосновения с раствором медного купороса. Мы видим, что измельчение вещества приводит к повышению скорости реакции.

Рис. 2. Результаты опыта по взаимодействия железного гвоздя и железного порошка с раствором CuSO4
ОПЫТ № 3. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ КОНЦЕНТРАЦИИ ИСХОДНЫХ ВЕЩЕСТВ
В две пробирки поместим по 2 гранулы цинка и осторожно прильем растворы уксусной кислоты: в первую пробирку – 9%-ный уксус, а во вторую – 70%-ную кислоту. Реакция протекает быстрее в той пробирке, в которой больше концентрация уксусной кислоты.
ОПЫТ № 4. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ
В две пробирки с соляной кислотой одинаковой концентрации добавим по 1 грануле цинка. Одну из пробирок поместим в стакан с горячей водой. Наблюдаем, что при нагревании скорость выделения водорода увеличивается. Скорость реакции зависит от температуры, при которой она проводится.
ОПЫТ № 5. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ УЧАСТИЯ КАТАЛИЗАТОРА
На дно стакана нальем 3%-ный раствор перекиси водорода. Пероксид водорода – очень непрочное вещество и легко разлагается на воду и кислород:
2H2O2 = 2H2O + O2↑.
При обычных условиях реакция разложения пероксида водорода протекает медленно, признаков реакции (т. е. выделения пузырьков газа) мы не наблюдаем. Добавим в стакан с перекисью водорода немного черного порошка оксида марганца (IV). Наблюдаем интенсивное выделение пузырьков газа. Внесем в стакан тлеющую лучинку – она разгорается, следовательно, выделяющийся газ – кислород. Почему при внесении в стакан оксида марганца скорость реакции увеличилась? Дело в том, что оксид марганца является катализатором реакции разложения пероксида водорода. Катализатор, участвуя в реакции, ускоряет ее, но сам в ней не расходуется.

Рис. 3. Разложение пероксида водорода под действием катализатора MnO2
Задача №1
Реакция протекает по уравнению А+В = 2С. Начальная концентрация вещества А равна 0,22 моль/л, а через 10 с — 0,215 моль/л. Вычислите среднюю скорость реакции.
Решение:
Используем формулу для расчёта
υ = ± ΔС/Δτ = ± (0,215-0,22)/(10-0) = 0,0005 моль/л ∙ с
Задача №2
Вычислите, во сколько раз увеличится скорость реакции при повышении температуры от 30 до 70 ∘ С, если температурный коэффициент скорости равен 2.
Решение:
По правилу Вант-Гоффа
υ=υ0·γ (t2-t1)/10
По условию задачи требуется определить υ/υ0:
υ/υ0=2 (70-30)/10 = 24 = 16
Задача №3
Запишите кинетическое уравнение для следующих уравнений реакций:
А) S(тв) + O2 (г) = SO2 (г)
Б) 2SO2 (г) + O2 (г) = 2SO3 (ж)
Решение:
Согласно закону действующих масс, который действует для газов и жидкостей:
υ = к1 C (O2)
υ = к2 C2(SO2)·C (O2)
Задача №4
Как изменится скорость реакции:
S (тв) + O2 (г) = SO2 (г)
при увеличении давления в системе в 4 раза?
Решение:
- Запишем кинетическое уравнение для реакции до повышения давления в системе. Обозначим концентрацию кислорода
С(О2) = а, концентрация серы - твёрдого вещества не учитывается.
υ = к1 а
- При повышении давления в 4 раза, объём уменьшается в 4 раза, следовательно концентрация газа кислорода увеличится в 4 раза и кинетическое уравнение примет вид:
υ' = к1 4а
- Определяем, во сколько раз возрастёт скорость реакции:
Задача №5
Как изменится скорость реакции:
2SО2 (г) + O2 (г) = 2SO3 (г)
при увеличении давления в системе в 2 раза?
Решение:
- Запишем кинетическое уравнение для реакции до повышения давления в системе. Обозначим концентрацию SO2
С(SО2) = а, концентрация кислорода C(O2) = b.
υ = к1 а2·b
- При повышении давления в 2 раза, объём уменьшается в 2 раза, следовательно концентрация газа кислорода и SO2 увеличится в 2 раза и кинетическое уравнение примет вид:
υ' = к1 (2а)2·2b = к14а2·2b= к18а2·b
- Определяем, во сколько раз возрастёт скорость реакции:
При температуре 10 ºС реакция протекает за 5 мин, при 20ºС – за 1 мин. Рассчитайте температурный коэффициент скорости реакции.
Дано: t0= 10 ºС t= 20ºС τ0= 300c τ= 60c |
γ=? |
Решение:
1) При условии, что концентрация вещества (С), вступившего в реакцию, постоянна:
При температуре 10 ºС скорость реакции равна υ0=∆C/∆τ0,
υ0=∆C/300, ∆C= 300υ0
При температуре 30 ºС скорость реакции равна υ=∆C/∆τ,
υ=∆C/60, ∆C= 60υ. Следовательно, 300υ0=60υ, а υ/υ0=300/60=5.
2) По правилу Вант Гоффа: υ= υ0γ∆t/10, υ/υ0= γ∆t/10
3) Согласно рассуждениям (1) и (2), получим γ(20-10)/10= γ=5
ТЕМА:Обратимость химических реакций. Обратимые и необратимые реакции. Реакции, идущие с образованием осадка, газа или воды. |
Обратимость химических реакций. Обратимые и необратимые реакции. Реакции, идущие с образованием осадка, газа или воды. Химическое равновесие и способы его смещения. Обратимые и необратимые химические реакции. Химическое равновесие и способы его смещения ПОНЯТИЕ ПРЯМОЙ И ОБРАТНОЙ РЕАКЦИИРассмотрим некоторую абстрактную реакцию, которую запишем в виде: А+В→АВ, Прямая реакция. Но многие химические реакции могут идти в обратную сторону. АВ Для краткости такую реакцию записывают, используя две стрелки, одну – вперед, другую – назад. А+В При повышении температуры скорость большинства химических реакций увеличивается. Но оказывается, что в случае некоторых реакций продукт реакции при температуре, когда она идет с хорошей скоростью, уже начинает разлагаться. В частности, такая ситуация реализуется при взаимодействии водорода с йодом при получении йодоводорода. Н2 + I2 Скорость химической реакции увеличивается с увеличением концентрации исходных веществ и соответственно уменьшается с уменьшением концентрации исходных веществ. Получается, что, по мере прохождения реакций, скорость прямой реакции будет уменьшаться, т. к. исходные вещества будут расходоваться. А скорость обратной реакции будет возрастать, потому что концентрация вещества АВ исходного для обратной реакции будет постепенно увеличиваться. До каких пор скорость прямой реакции будет уменьшаться, а обратной увеличиваться? Это будет до того момента, когда скорости прямой и обратной реакции станут равными. Наступит химическое равновесие. Рис. 1.
Рис. 1 Химическое равновесие – это состояние реакционной системы, в котором скорости прямой и обратной реакции равны. КОНСТАНТА РАВНОВЕСИЯРавновесная концентрация веществ Равновесная концентрация веществ – это концентрации веществ в реакционной смеси, находящихся в состоянии химического равновесия. Равновесная концентрация обозначается химической формулой вещества, заключенной в квадратные скобки. Например, следующая запись
Рис. 2 Химическое равновесие (Рис. 2) отличается от привычного для нас понятия «равновесие». Химическое равновесие – динамическое. В системе, находящейся в состоянии химического равновесия, происходят и прямая, и обратная реакции, но их скорости равны, и поэтому концентрации участвующих веществ не меняются. Химическое равновесие характеризуется константой равновесия, равной отношению констант скоростей прямой и обратной реакций.
Константы скорости прямой и обратной реакции – это скорости данной реакции при концентрациях исходных для каждой из них веществ в равных единицах. Также константа равновесия равна отношению равновесных концентраций продуктов прямой реакции в степенях стехиометрических коэффициентов к произведению равновесных концентраций реагентов.
Если ОБРАТИМЫЕ И НЕОБРАТИМЫЕ ХИМИЧЕСКИЕ РЕАКЦИИЕсли константа равновесия значительно больше 1, такую реакцию называют необратимой. Необратимыми называются химические реакции, которые происходят только в одном направлении до полного расходования одного из реагентов. Например, это реакция: 4Р+5О2 =2Р2О5 (2) Обратимыми называются химические реакции, которые осуществляются во взаимно противоположных направлениях при одних и тех же условиях. ФАКТОРЫ, ВЛИЯЮЩИЕ НА СМЕЩЕНИЕ РАВНОВЕСИЯЕсли изменить внешние условия, то состояние химического равновесия нарушится. Смещение равновесия в зависимости от изменения внешних условий в общем виде определяется · Принципом Ле Шателье: если на систему, находящуюся в равновесии, оказывают воздействие извне путем изменения какого-либо из условий, определяющих положение равновесия, то оно смещается в направлении того процесса, протекание которого ослабляет эффект произведённого воздействия. Так, повышение температуры вызывает смещение равновесия в направлении того из процессов, течение которого сопровождается поглощением тепла, а понижение температуры действует в противоположном направлении. Равновесие смещается вправо, если повысились равновесные концентрации продуктов прямой реакции. Если повышаются равновесные концентрации исходных веществ прямой реакции, то равновесие смещается влево. Какие факторы можно изменять, чтобы сместить равновесие? Это · Температура · Давление · Концентрации веществ · Добавление катализатора · Изменение площади реакционной поверхности гетерогенных реакций Добавление катализатора и изменение площади реакционной поверхности гетерогенных реакций не оказывают влияние на смещение химического равновесия.
Остальные факторы рассматриваем более детально. Температура Реакция синтеза аммиака (Рис. 3) относится к экзотермическим реакциям. При прохождении прямой реакции теплота выделяется, а при прохождении обратной – поглощается. Если увеличить температуру, то, согласно правилу Ле Шателье, равновесие сместится в таком направлении, чтобы уменьшить это воздействие. В данном случае влево, так как теплота поглощается. Реакция синтеза аммиака проводится при температуре около 500 Если реакция эндотермическая, то повышение температуры приведет к смещению равновесия вправо. Изменение концентрации веществ При увеличении концентрации какого-либо из веществ, участвующих в равновесной реакции, равновесие реакции сместится в сторону его расходования, а соответственно, при уменьшении концентрации какого-либо из веществ – в сторону реакции его образования. Например, при увеличении концентрации азота в реакции синтеза аммиака, равновесие сместится вправо, т. е. в сторону расходования азота. Если же в этой реакции удалять из реакционной смеси аммиак, то равновесие сместится в сторону его образования. Сделать это можно, например, при растворении аммиака в воде. Изменение давления Изменение давления может оказывать влияние только на реакции с участием газообразных веществ. Если в реакции синтеза аммиака увеличить давление, равновесие сместится в сторону уменьшения числа моль газа. Если слева число моль газа больше, чем справа, равновесие сместится в сторону образования аммиака. Если число моль газа одинаково и слева и справа, например, в реакции получения оксида азота (II), N2 +O2 то изменение давления не будет оказывать влияние на положение химического равновесия в таких реакциях. Изучение химического равновесия имеет большое значение, как для теоретических исследований, так и для решения практических задач. Определяя положение равновесия для различных температур и давлений, можно выбрать наиболее благоприятные условия проведения химического процесса. Окончательный выбор условий требует учета влияния их и на скорость процесса. Подведение итога урока На уроке была изучена тема «Химическое равновесие», рассмотрены условия смещения равновесия в случае обратимых реакций. ГРУППА 508 ХИМИЯ ТЕМА: Свойства карбоновых кислот. (НЕ ПИШИТЕ ВСЕ ПОДРЯД! ЧИТАЙТЕ, ДЕЛАЙТЕ КРАТКИЙ КОНСПЕКТ, УДЕЛИТЕ ВНИМАНИЕ ХИМИЧЕСКИМ РЕАКЦИЯМ)
Общая формула предельных одноосновных карбоновых кислот: СnH2nO2 Строение, изомерия и гомологический ряд карбоновых кислот Химические свойства карбоновых кислот Классификация карбоновых кислот ПО ЧИСЛУ КАРБОКСИЛЬНЫХ ГРУПП:
КЛАССИФИКАЦИЯ ПО СТРОЕНИЮ УГЛЕВОДОРОДНОГО РАДИКАЛА
Строение карбоновых кислотКарбоксильная группа сочетает в себе две функциональные группы – карбонил и гидроксил, взаимно влияющие друг на друга.
Электронная плотность смещена к более электроотрицательному атому кислорода. Атом углерода карбоксильной группы находится в состоянии sp2-гибридизации, образует три σ-связи и одну π-связь. Водородные связи и физические свойства карбоновых кислотВ жидком состоянии и в растворах молекулы карбоновых кислот образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул карбоновых кислот. Молекулы карбоновых кислот с помощью водородных связей соединены в димеры.
Это приводит к увеличению растворимости в воде и высоким температурам кипения низших карбоновых кислот. С увеличением молекулярной массы растворимость кислот в воде уменьшается.
Номенклатура карбоновых кислот
Предельные одноосновные карбоновые кислоты.
Таблица. Непредельные одноосновные карбоновые кислоты.
Таблица. Двухосновные карбоновые кислоты.
Таблица. Ароматические карбоновые кислоты.
Изомерия предельных карбоновых кислотСТРУКТУРНАЯ ИЗОМЕРИЯДля предельных карбоновых кислот характерна структурная изомерия – изомерия углеродного скелета и межклассовая изомерия. Структурные изомеры – это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул. Изомеры углеродного скелета характерна для карбоновых кислот, которые содержат не менее четырех атомов углерода.
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Карбоновые кислоты изомерны сложным эфирам. Общая формула и спиртов, и простых эфиров — CnH2nО2.
Общую формулу СnH2nO2 могут также иметь многие другие полифункциональные соединения, например: альдегидоспирты, непредельные диолы, циклические простые диэфиры и т.п.
|
ТЕМА:Д
Вариант 1
1. Одноосновная бескислородная кислота
А) H2S Б) H2CO3 В) HF Г) HNO3
2. Сумма коэффициентов в полном ионном уравнении BaCl2 + H2SO4=
А) 11 Б) 10 В) 7 Г) 9
3. Коэффициенты перед AlCL3 и NH4Cl в уравнении реакции NH4NO3 + AlCL3 = Al(NO3)3 + NH4Cl соответственно равны…
А) 1 и 2 Б) 1 и 3 В) 3 и 1 Г) 2 и 1
4. Элементы только побочных подгрупп находятся в ряду
А) Sc, Mo, W Б) Ta, Ca, Mn В) As, Br, Cr Г) Sb, Co, Ge
5. Металлические свойства убывают в ряду
А) Ge, Sn, Pb Б) Sr, Y, Mo В) Tc, Nb, Sr Г) K, Rb, Cs
6. Самый активный неметалл
А) At Б) F В) B Г) Si
7. Максимальная валентность атома Se равна
А) 2 Б) 4 В) 8 Г) 6
8. Относительная молекулярная масса K2S
А) 71 Б) 110 ат. ед. м. В) 110 Г) 71 ат. ед. м.
9. Электронное строение атома калия соответствует выражению
А) 1S22S22P63S23P64S1 Б) 1S22S22P63S23P63d1
В) 1S22S22P63S23P7 Г) 1S22S22P63S23P64S2
10. Количество элементов в 5 периоде
А) 18 Б) 32 В) 8 Г) 24
11. Максимальное число электронов на р-орбиталях:
А) 2; Б) 6; В) 10; Г) 14.
12. Число нейтронов в атоме цинка равно:
А) 65; Б) 22; В) 30; Г) 35.
13. В периоде слева направо уменьшается
А) число уровней Б) число валентных электронов
В) радиус атома Г) активность неметаллов
14. Степень окисления атома углерода в соединении Ca(ClO2)2 равна
А ) -4 Б) -3 В) +4 Г) +3
15. Сумма коэффициентов в полном ионном уравнении реакции взаимодействия хлорида кальция и нитрата серебра
А) 10 Б) 8 В) 14 Г) 12
16. Сокращённое ионное уравнение: Fe2+ + 2OH- = Fe (OH)2 соответствует взаимодействию
А) FeCO3 + 2NaOH В) Fe(NO3)2 + 2NaOH С) FeSiO3 + LiOH
D) FeCl2 + Cu(OH)2 Е) FeS+ 2KOH
17. Изомером бутина-1 является вещество:
A) СН2=СН - С2Н5
Б) СН3 – СН – СН3
׀
СН3
В) НС ≡С – С2Н5
Г) Н2С = СН – СН2 – СН3
18. При повышении давления химическое равновесие сместится в сторону исходных веществ в системе…
А)2SO2 + O2
Б) CH4 + H2O
В) CO + 2H2
Г) 4HCl + O2
19. «Бесцветная жидкость с резким запахом, легче воды, хорошо растворим в воде, гигроскопичен, обладает бактерицидными свойствами» - данные свойства соответствуют:
А) бензол Б) этиловый спирт В) сахароза Г) бензол
20. Название вещества
а) 3 метал 5 пропил гептан б) 3 пропил 5 метил гептен3
в) 3 пропил 5 метил гептан г) 2, 5 диметил 3этил гептен 3
21. (Выбрать несколько вариантов ответа)С какими веществами взаимодействует HNO3
а) HCL б) Mg в) P2O5 г) Fe2O3
22. (Выбрать несколько вариантов ответа)Выбрать кислоты:
А) MgCl2 Б) Al(OH)3 В) H3PO4 Г) HF Д) NaOH Е) CO2
23. (Выбрать несколько вариантов ответа)Прочитать текст.
Для изготовления активированного угля используют различные углеродсодержащие материалы органического происхождения: торф, каменноугольный кокс, древесный и коксовый угли. В результате получают вещество, обладающее высокими адсорбирующими и каталитическими свойствами. Именно большое количество пор обуславливает мощную впитывающую способность активированного угля, который используют для поглощения токсических веществ, газообразных соединений. Однако при этом уголь слабо поглощает такие соединения, как щелочи и кислоты. Использование активированного угля эффективно впервые 12 часов после отравления. При отравлении, в том числе тяжелом, активированный уголь нужно принимать еще до промывания желудка. Принимать уголь нужно в расчете 1 таблетка на 10 кг веса. Попадая в организм уголь, подобно губке, впитывает в себя вредные вещества и спустя некоторое время естественным путем выводится вместе с ними.
Выбрать истинные суждения, согласно тексту.(Ответов несколько)
А) Активированный уголь делают из древесного угля
Б) Лучше всего уголь использовать после промывания желудка
В) Активированный уголь эффективен при любых отравлениях
Г) Для подростка весом 60кг нужно выпить 3 таблетки угля
Д) Для подростка весом 60кг нужно выпить 6 таблеток угля
Е) Активированный уголь является адсорбентом
Ж) Эффективнее использовать порошок угля чем таблетки
Часть В
1. Соотнести виды химической связи и формулу вещества
1) ковалентная полярная
2) ионная
А) NaCl Б) HCl В) Mg(OH)2 Г) Cl2 Д) NO2
Ответ оформите в виде таблицы:
1 | 2 |
|
|
2. Соотнести название продукта и тип дисперсной системы:
1) суспензия
2) порошок
3) гель
А) мука Б) компот В) цукаты Г) холодец
Ответ оформите в виде таблицы:
1 | 2 | 3 |
|
|
|
3.Соотнести формулы веществ и класс углеводородов. Ответ представить в виде таблицы.
Формулы Класс углеводородов
А) С4Н10 1) Алканы
Б) С6Н12 2) Алкены
В) С2Н6 3) Алкины
Г) С4Н8
Д) С8Н16
Е) С5Н8
Часть С
21. В 15%-ном раствор кислоты массой 300 г добавили 30г. Рассчитайте массовую долю серной кислоты в полученном растворе.
30.Записать два изомера и два гомолога для 2- метил пентана
31.Осуществить схему превращений:
CH3 ─ CH3 → CH2 ═CH2 → CH ≡CH
ГРУППА 508 ХИМИЯ 60
ТЕМА:Химические свойства карбоновых кислот.
Для карбоновых кислот характерны следующие свойства:
|
1. Кислотные свойства
| Кислотные свойства карбоновых кислот возникают из-за смещения электронной плотности к карбонильному атому кислорода и вызванной этим дополнительной (по сравнению со спиртами и фенолами) поляризацией связи О–Н. |
| Карбоновые кислоты – кислоты средней силы. В водном растворе карбоновые кислоты частично диссоциируют на ионы: R–COOH ⇆ R-COO– + H+ |
1.1. Взаимодействие с основаниями
Карбоновые кислоты реагируют с большинством оснований. При взаимодействии карбоновых кислот с основаниями образуются соли карбоновых кислот и вода.
CH3COOH + NaOH = CH3COONa + H2O
Карбоновые кислоты реагируют с щелочами, амфотерными гидроксидами, водным раствором аммиака и нерастворимыми основаниями.
| Например, уксусная кислота растворяет осадок гидроксида меди (II) |
Видеоопыт взаимодействия уксусной кислоты с гидроксидом натрия можно посмотреть здесь.
| Например, уксусная кислота реагирует с водным раствором аммиака с образованием ацетата аммония |
CH3COOH + NH3 = CH3COONH4
1.2. Взаимодействие с металлами
Карбоновые кислоты реагируют с активными металлами. При взаимодействии карбоновых кислот с металлами образуются соли карбоновых кислот и водород.
| Например, уксусная кислота взаимодействует с кальцием с образованием ацетата кальция и водорода. |
![]()
Видеоопыт взаимодействия уксусной кислоты с магнием и цинком можно посмотреть здесь.
1.3. Взаимодействие с основными оксидами
Карбоновые кислоты реагируют с основными оксидами с образованием солей карбоновых кислот и воды.
| Например, уксусная кислота взаимодействует с оксидом бария с образованием ацетата бария и воды. |
![]()
| Например, уксусная кислота реагирует с оксидом меди (II) |
2СН3СООН + CuO = H2О + ( CH3COO)2 Cu
Видеоопыт взаимодействия уксусной кислоты с оксидом меди (II) можно посмотреть здесь.
1.4. Взаимодействие с с солями более слабых и летучих (или нерастворимых) кислот
Карбоновые кислоты реагируют с солями более слабых, нерастворимых и летучих кислот.
| Например, уксусная кислота растворяет карбонат кальция |
![]()
| Качественная реакция на карбоновые кислоты: взаимодействие с содой (гидрокарбонатом натрия) или другими гидрокарбонатами. В результате наблюдается выделение углекислого газа |
![]()
2. РЕАКЦИИ ЗАМЕЩЕНИЯ ГРУППЫ ОН
| Для карбоновых кислот характерны реакции нуклеофильного замещения группы ОН с образованием функциональных производных карбоновых кислот: сложных эфиров, амидов, ангидридов и галогенангидридов. |
2.1. Образование галогенангидридов
Под действием галогенагидридов минеральных кислот-гидроксидов (пента- или трихлорид фосфора) происходит замещение группы ОН на галоген.
| Например, уксусная кислота реагирует с пентахлоридом фосфора с образованием хлорангидрида уксусной кислоты |

2.2. Взаимодействие с аммиаком
При взаимодействии аммиака с карбоновыми кислотами образуются соли аммония:

При нагревании карбоновые соли аммония разлагаются на амид и воду:

2.3. Этерификация (образование сложных эфиров)
Карбоновые кислоты вступают в реакции с одноатомными и многоатомными спиртами с образованием сложных эфиров.
| Например, этанол реагирует с уксусной кислотой с образованием этилацетата (этилового эфира уксусной кислоты): |
При этом фенол не вступает в реакцию этерификации с карбоновыми кислотами. Сложные эфиры фенола получают косвенными способами.
2.4. Получение ангидридов
С помощью оксида фосфора (V) можно дегидратировать (то есть отщепить воду) карбоновую кислоту – в результате образуется ангидрид карбоновой кислоты.
| Например, при дегидратации уксусной кислоты под действием оксида фосфора образуется ангидрид уксусной кислоты |

3. ЗАМЕЩЕНИЕ АТОМА ВОДОРОДА ПРИ АТОМЕ УГЛЕРОДА, БЛИЖАЙШЕМ К КАРБОКСИЛЬНОЙ ГРУППЕ
| Карбоксильная группа вызывает дополнительную поляризацию связи С–Н у соседнего с карбоксильной группой атома углерода (α-положение). Поэтому атом водорода в α-положении легче вступает в реакции замещения по углеводородному радикалу. |
В присутствии красного фосфора карбоновые кислоты реагируют с галогенами.
| Например, уксусная кислота реагирует с бромом в присутствии красного фосфора |

4. СВОЙСТВА МУРАВЬИНОЙ КИСЛОТЫ
| Особенности свойств муравьиной кислоты обусловлены ее строением, она содержит не только карбоксильную, но и альдегидную группу и проявляет все свойства альдегидов. |

4.1. Окисление аммиачным раствором оксида серебра (I) и гидроксидом меди (II)
Как и альдегиды, муравьиная кислота окисляется аммиачным раствором оксида серебра. При этом образуется осадок из металлического серебра.

При окислении муравьиной кислоты гидроксидом меди (II) образуется осадок оксида меди (I):

4.2. Окисление хлором, бромом и азотной кислотой
Муравьиная кислота окисляется хлором до углекислого газа.

4.3. Окисление перманганатом калия
Муравьиная кислота окисляется перманганатом калия до углекислого газа:
5HCOOH + 2KMnO4 + 3H2SO4 → 5CO2 + 2MnSO4 + K2SO4 + 8H2O
Видеоопыт взаимодействия муравьиной кислоты с перманганатом калия можно посмотреть здесь.
4.4. Разложение при нагревании
При нагревании под действием серной кислоты муравьиная кислота разлагается с образованием угарного газа:

Видеоопыт разложения муравьиной кислоты
5. ОСОБЕННОСТИ БЕНЗОЙНОЙ КИСЛОТЫ
5.1. Разложение при нагревании
При нагревании бензойная кислота разлагается на бензол и углекислый газ:

5.2. Реакции замещения в бензольном кольце
| Карбоксильная группа является электроноакцепторной группой, она уменьшает электронную плотность бензольного кольца и является мета-ориентантом. |

6. ОСОБЕННОСТИ ЩАВЕЛЕВОЙ КИСЛОТЫ
6.1. Разложение при нагревании
При нагревании щавелевая кислота разлагается на угарный газ и углекислый газ:

6.2. Окисление перманганатом калия
Щавелевая кислота окисляется перманганатом калия до углекислого газа:

7. ОСОБЕННОСТИ НЕПРЕДЕЛЬНЫХ КИСЛОТ (АКРИЛОВОЙ И ОЛЕИНОВОЙ)
7.1. Реакции присоединения
Присоединение воды и бромоводорода к акриловой кислоте происходит против правила Марковникова, т.к. карбоксильная группа является электроноакцепторной:

К непредельным кислотам можно присоединять галогены и водород. Например, олеиновая кислота присоединяет водород:

7.2. Окисление непредельных карбоновых кислот
Непредельные кислоты обесцвечивают водный раствор перманганатов. При этом окисляется π-связь и у атомов углерода при двойной связи образуются две гидроксогруппы:

Получение карбоновых кислот
1. ОКИСЛЕНИЕ СПИРТОВ, АЛКЕНОВ И АЛКИНОВ
При окислении спиртов, алкенов, алкинов и некоторых других соединений подкисленным раствором перманганата калия образуются карбоновые кислоты.
| Например, при окислении этанола в жестких условиях образуется уксусная кислота |

2. ОКИСЛЕНИЕ АЛЬДЕГИДОВ
Альдегиды реагируют с раствором перманганата или дихромата калия в кислой среде при нагревании, а также с гидроксидом меди при нагревании.
| Например, при окислении уксусного альдегида перманганатом калия в серной кислоте образуется уксусная кислота. |

| Например, при окислении альдегидов гидроксидом меди (II) также образуются карбоновые кислоты |

3. ЩЕЛОЧНОЙ ГИДРОЛИЗ ТРИГАЛОГЕНИДОВ
Тригалогеналканы, в которых три атома галогена расположены у одного атома углерода, с избытком щелочи образуется соль кислоты. При этом сначала происходит замещение галогенов на группы ОН.

Образуется неустойчивое вещество, которое распадается с отщеплением воды:

Так как щелочь в избытке, то образуется не сама кислота, а её соль:

4. ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ ИЗ СОЛЕЙ
Карбоновые кислоты можно получить из солей действием минеральной кислоты на раствор соли:

| Например, муравьиную кислоту можно получить, подействовав на формиат натрия раствором серной кислоты: |
![]()
5. ГИДРОЛИЗ СЛОЖНЫХ ЭФИРОВ
Сложные эфиры подвергаются гидролизу в кислой среде при нагревании:

| Например, метилацетат гидролизуется в кислой среде: |

6. Кислотный гидролиз жиров
Под действием кислот жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
| Например, при гидролизе тристеарата глицерина в кислой среде образуется стеариновая кислота и глицерин |

7. ПОЛУЧЕНИЕ МУРАВЬИНОЙ КИСЛОТЫ ИЗ УГАРНОГО ГАЗА
Соль муравьиной кислоты получают нагреванием оксида углерода (II) с твёрдым гидроксидом натрия под давлением:

8. КАТАЛИТИЧЕСКОЕ ОКИСЛЕНИЕ БУТАНА
Уксусную кислоту в промышленности получают каталитическим окислением бутана:
![]()
9. ПОЛУЧЕНИЕ БЕНЗОЙНОЙ КИСЛОТЫ
Бензойную кислоту получают окислением гомологов бензола раствором перманганата калия в кислой среде.
| Например, при окислении толуола образуется бензойная кислота: |

10. ВЗАИМОДЕЙСТВИЕ РЕАКТИВА ГРИНЬЯРА С УГЛЕКИСЛЫМ ГАЗОМ
При взаимодействии реактивов Гриньяра (алкилгалогенидов магния) с углекислым газом и последующем гидролизе образовавшегося промежуточного продукта образуется карбоновая кислота.





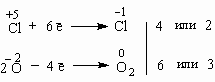
















Комментариев нет:
Отправить комментарий